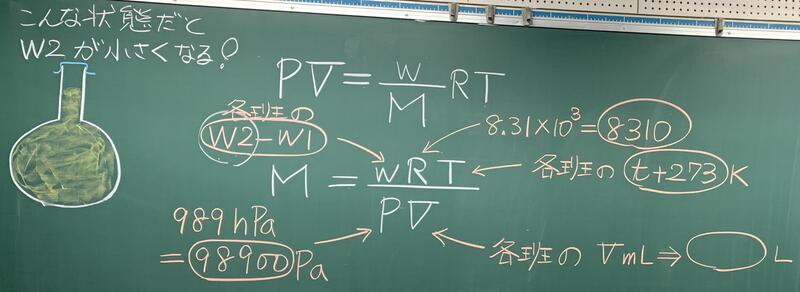理科のこと、環境ニュース
なかなか上手でしょう? 空気砲の演示!!
生徒たちが自分たちだけで作り上げた「空気砲」です!
これまでは、結果が良く分からないものばかりでした。
今回のは期待を上回る出来で、ビックリ!!
今回の空気砲の特徴ですが、
① 箱本体が大きい
1辺が90センチほどの立方体の箱になってる
② 本体はいつもの段ボールじゃない
プラ段つまりプラスチックダンボール製
この空気砲本体のプラ段は、ホームセンターで1畳サイズのプラ段を半分サイズにカットしたものです。
これを1人で抱えて持ってきたとのこと。
この90センチ平方のプラ段6個を、養生テープでしっかりと貼り合わせて箱に作ってあります。
空気を噴出させる穴はコンパス型のカッターでキレイに開けてあります。
この箱に煙を貯めて、箱の1つの面を叩くと、穴からドーナツ状の煙が飛び出してきます。
今回の様子を良く見てみると、
プラ段は紙の段ボールよりかなり大きくしなるので、一気に大量の空気を穴から押し出せるんですね!
しかも箱を大きい体積で作ってあることも大量の空気を押し出せる要因になっているんです。
色んなものを参考にしながら、自力で考えて仕上げたとのこと。
すごく感心しました!!
★空気砲について
段ボールの箱を両手でたたくと、
勢いよく飛び出した煙はドーナツ状のかたまりとなって飛んでいく。
そのスピードと、身体に当たったときの意外に大きい衝撃に驚くこと間違いなし!
風に吹かれるのとは違う、空気の弾丸があたった感じ。
空気中を空気がかたまりとなって飛ぶ、そんなことがどうして起きるのでしょうか?
空気は、「流体」の一種で、一定の形を取らず自由に変形する。
その流体に特徴的な現象が「渦」。
空気のかたまりの正体は、空気の渦、しかも渦の管がドーナツ状に閉じたもので、
自然界ではめったに目にすることのない「渦輪」なのです。
流体要素の角運動保存則から、いったんできた渦はなかなか消滅しないんですね!
それで、このような印象的な演示を見ることが出来るのです。
揮発性物質の分子量測定 誤差の原因
気体の状態方程式の勉強のあとに、物質の分子量測定という項目が出てきます。
その中で、液体物質の分子量を測定する実験があります。
液体物質を加熱して蒸発させて気体とし、気体となった物質の、質量、温度、圧力を測定します。
この測定値を状態方程式に代入して計算すると、分子量が求められます!
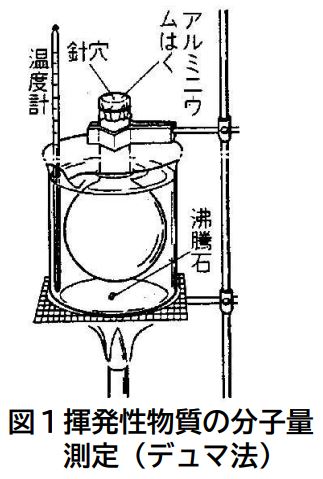
実験装置は以下のようです。
この実験をヘキサンC6H14について、何回かやってみました。
下の写真のようにフラスコの底に液体が確認出来ます。
この状態を目視するのがかなり大変です。
蒸発し切ったかどうかの確認が難しいんです
液体が全て蒸発してから2分ほど温度を変えずに加熱を続けます。
この時の加熱時間は長すぎてもいけません。
下の写真では、液体が蒸発してフラスコ上部で再び液化してフラスコ下部に戻る「還流」が確認出来ますが、
この還流も起こらなくなるまで加熱を続けます。
さて、何回か行った実験の全ての回で、実験値が理論値に対して10~15%ほど小さく出てしまいました。
誤差の原因を何度も考えてみましたが、最もそれらしいと思えたのは、
気体となった物質を捕集する時の失敗です。
① 加熱時間が長すぎた
② 加熱時に一時的に温度が上がり過ぎ、その後温度が下がった
③ アルミ箔のフタの密閉性が悪く、気体が逃げた
これらのいずれもが、気体がフラスコの外に逃げてしまい、気体の測定質量が小さくなってしまう原因になります。
この状態で以下のように計算すると、求まる分子量の値は小さくなってしまいます。
気温が板書してありますが、計算式中で使う温度はフラスコを温める湯の温度(絶対温度)を用います。
フラスコ内部の温度を測るのが理想ですが、出来るだけフラスコの密閉性を保ちたいので難しいでしょう。
今と昔でちがう「理科の学習」びっくりランキング
第1位:アルコールランプは使用しなくなった
アルコールランプは、理科の授業では見る機会が減っています。
より扱いやすく安全な、カセットガスコンロを使うようになっているようです。
第2位:カエルの解剖の代わりにイカの解剖をするようになった
現在では、準備や後片づけに手間がかかることや、動物愛護の観点から解剖は行わないことが多いそうです。
しかし、2010年代の教科書に「無脊椎動物」の項目が復活した影響で「イカの解剖」をすることも増えているそうです。
第3位:冥王星が惑星から外れた
太陽系の惑星の覚え文句といえば、「水・金・地・火・木・土・天・海・冥」と習った人も多いかもしれません。
しかし、現在の太陽系の惑星は「海」まで。
2006年から冥王星は惑星の仲間から外されています。
国際会議で「太陽の周りを回っていること」「重力が強く丸い形をしていること」「周りに同じような天体が存在しないこと」などの定義が決まり、冥王星はこれを満たさなかったそうです。
そこで現在の教科書では、冥王星は太陽系の外側を回る「太陽系外縁天体」として扱われています。
第4位:富士山は活火山の扱いになった
日本最高峰の富士山。
現在は徐々に活火山としての認知が広まってきていますが、昔の教科書では「休火山」と記されていました。
活火山の扱いに変わったのは、2003年に活火山の定義が変更されたから。
2003年以前の活火山の定義は「活発な噴火活動があり、過去およそ2000年以内に噴火した火山」。
それに対して、2003年以降は「おおむね過去1万年以内に噴火した火山」とされました。
第5位:優性・劣性遺伝は顕性・潜性に言い換えている
メンデルがエンドウの実験から発見した遺伝の法則。
優性遺伝・劣性遺伝という用語も習いましたね。
ところが近年の教科書では、この用語が「顕性遺伝・潜性遺伝」と言い換えられているそうです。
理由は、遺伝子に優劣があるという誤解を与えないためなのだそうです。
第6位:SDGsの項目が追加された
SDGs(エス・ディー・ジーズ)は、Sustainable Development Goals(持続可能な開発目標)の略称。
令和3年に主要5教科すべての教科書に、SDGsの項目が追加されました。
第7位:哺乳類までの進化の過程の認識が変わった
両生類から分かれた哺乳類と爬虫類がそれぞれ進化し、爬虫類から進化したのが鳥類という説が有力になったため。
「哺乳類のルーツは両生類」が新常識となりました。
第8位:「化合」という語句を使わなくなった
化学変化の表現の正確性に欠けるとされ、ほとんど使わなくなりました。
第9位:「希ガス」から「貴ガス」表記になった
平成28年版教科書から、国際的にも一般的な呼び方とされる「貴ガス」の表記に変更されました。

第10位:「ダニエル電池」が登場した
令和3年度より、化学の電池の内容が一新されました。
衝撃! 「H3」1号機打ち上げ失敗
日本の新たな主力ロケット「H3」1号機が
7日午前10時37分頃、鹿児島県の種子島宇宙センターから打ち上げられたが、
第2段エンジンの着火が確認されず、
JAXAは約15分後、地上から指令破壊の信号を機体に送った。
打ち上げは失敗となった。
文部科学省は同日、原因究明のための対策本部を設置する。
現在の主力ロケット「H2A」の後継機となるH3は
低コスト化や打ち上げ能力の増強で世界の衛星打ち上げ市場に参画することが期待されていたが、
政府やJAXAには大きな打撃となる。
1号機は先月17日に打ち上げ直前に中止するトラブルに見舞われ、
再び打ち上げに臨んでいた。
前回は第1段の主エンジン着火後に異常を検知し、補助ロケットが着火しなかった。
原因調査の結果、電気的ノイズの影響で第1段の制御システムで誤動作が起きたことが判明。
ノイズを抑える対策を完了させたとしていた。
H3は、JAXAと三菱重工業などが14年から開発を進めてきた。
これまでの開発費は約2060億円に上る。
1号機には、災害時の被害状況把握などを行う政府の地球観測衛星「だいち3号」が搭載されており、
防災面などへの影響も必至だ。
三菱重工の元技師長で東京理科大の小笠原宏教授は
「第2段エンジンはH2Aとほぼ同じものを継承して使っており、ほとんど変えておらず、H2Aではこのようなトラブルはなかった。
なぜこのようなことになったのか全く分からない」
と困惑した様子で話した。
昨夜の月食はハッキリと見えたのでは?
11月8日夜の月食は、多くの地点でハッキリと見えたようですね。
ここ埼玉県入間市でもバッチリでした!
自分は、職場の屋上から見ていたんですが、
部分月食から皆既月食に移るところまでを見て、
その後急いで帰宅し、皆既月食の最大(最も暗くなるところ)を確認することが出来ました。
そして最後に部分月食の終わりの方を見たんです。
写真はスマホで撮ったんですが、やはり上手く写りません・・・
一応、載せてみますね。
<19時14分:部分食から皆既食に移るところ>
<19時16分:皆既食の始まり>
<19時45分:皆既食の最大付近>
<21時36分:部分食の終わり近く>

すみません。
差がほとんど分からないですね・・・
ネット上、Youtube等でキレイな画像がupされるはずですので、そちらを観て下さい。
天王星食についても、そこで確認出来ると思います。
今夜は皆既月食、天王星食が同時に! 442年ぶりの天体ショー!
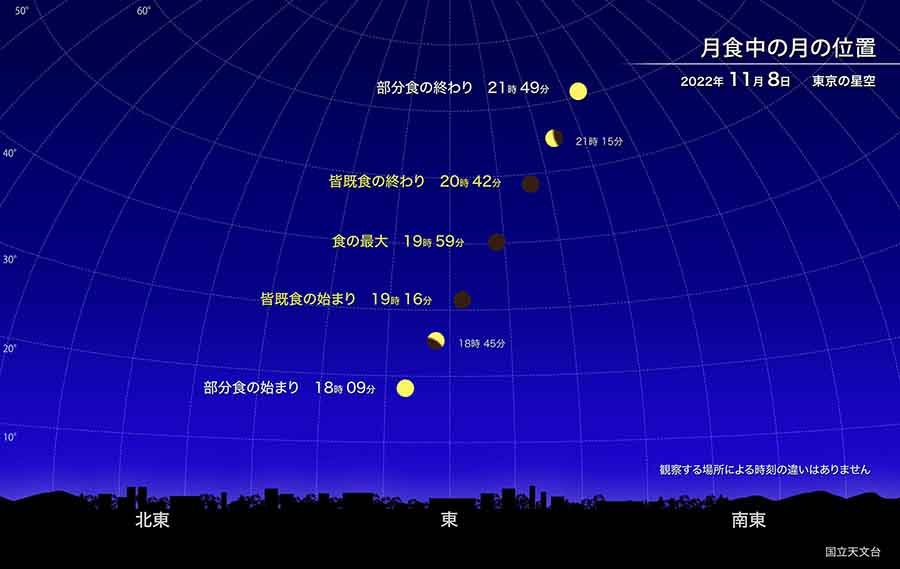
皆既月食は、月全体が地球の影に入り、
赤黒く変色した月が見られる天体現象。
今日は、午後6時9分に部分月食が始まり、
皆既月食の始まりは午後7時16分、
食の最大は午後7時59分で、
午後8時42分に皆既月食の終わりとなる。
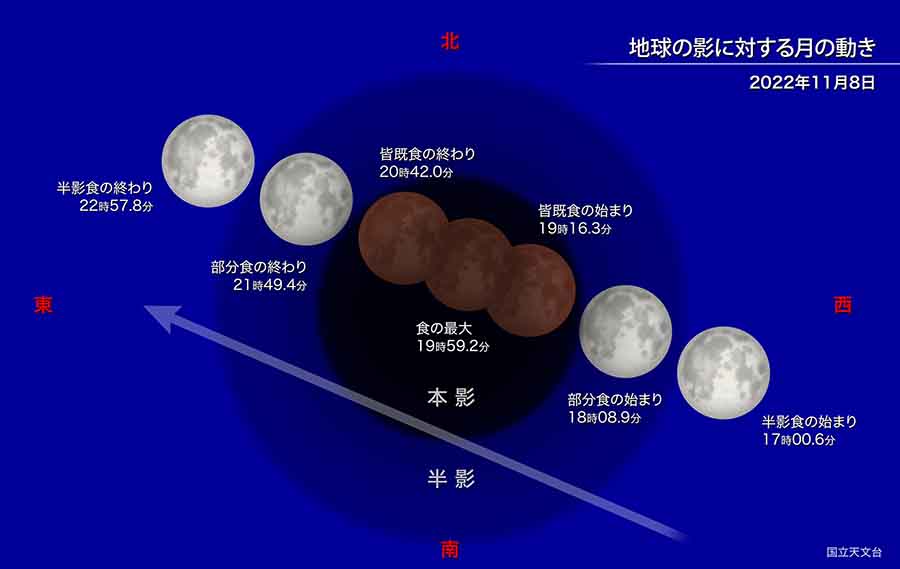
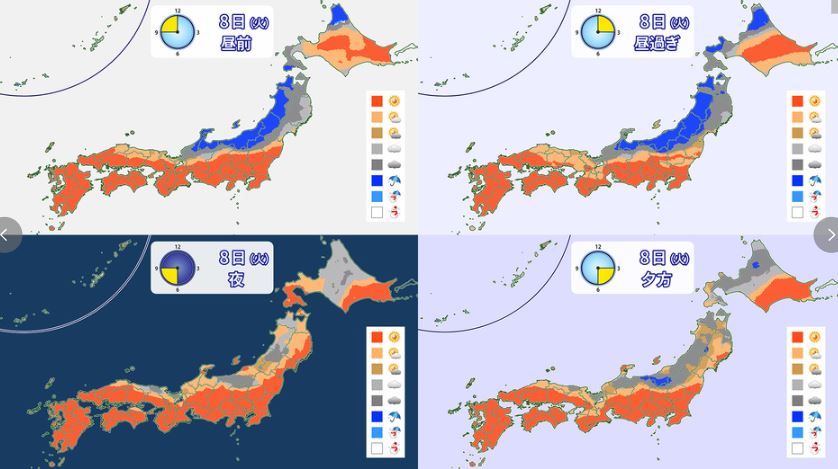
今回は、多くの地域で月の高度がある程度高くなる時間帯に皆既食となるため、
観察しやすいといえそうだ。
さらに今回は月食の最中、月に天王星が隠される「天王星食」も起こる。
皆既食中に天王星食が起こるのは非常に珍しく、
442年ぶりの貴重な天体ショーとなる。
(天王星は約6等級で、薄い青色に見えます。
条件が良くても肉眼で見える限界の明るさなので、双眼鏡や望遠鏡などで探してみましょう)
織田信長が観ていたかもしれないという観測が、今日出来るかも!
(気象予報士・多胡安那)
気体から固体への状態変化は「凝華」と呼ぶことに!
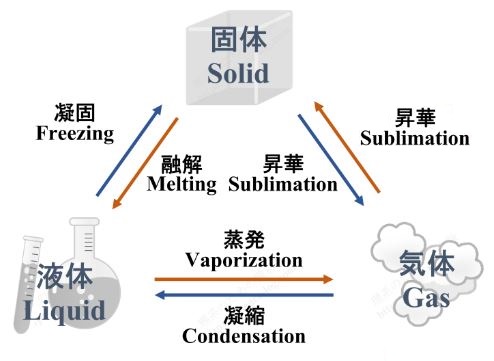
固体・液体・気体の三態間で状態変化する時の呼び方ですが、
つい最近までは、次のようでした。
ここで、固体から気体、気体から固体、どちらの変化も「昇華」と呼ぶようになってしまったのは、
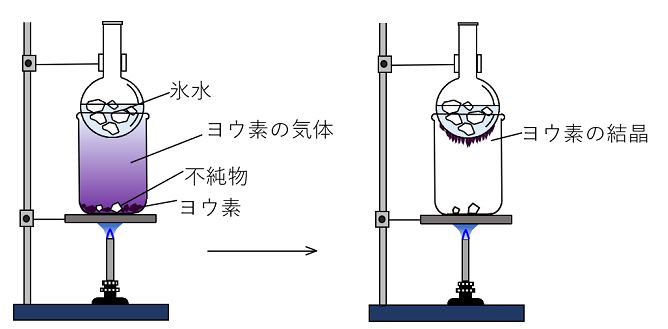
固体物質を精製する方法としての「いったん蒸気にしてふたたび固体にする」
ということをさしたことから来たものだと推測されています。
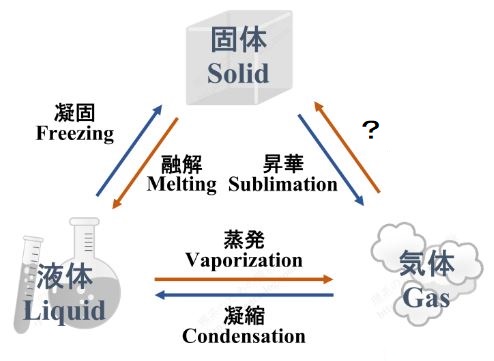
ですから、ここの2か所の変化の呼び方を別にするという改善をすべきだったんですね。
「昇華」という字は、固体から気体への変化にはあてられて良さそうです。
そこで、気体から固体への変化の呼び方を別に考えることになりました。
中国語では、気体から固体への変化をさす「凝華」という言い方があって、
最近は中国でも台湾でもこれを教えるようになっているそうです。
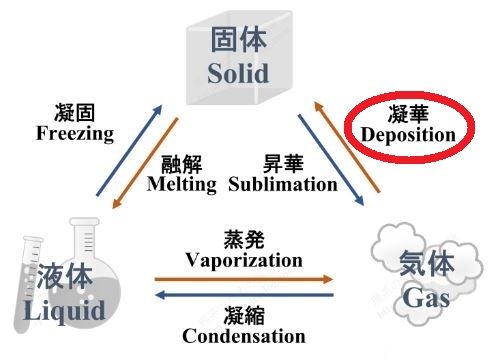
ということで、日本語でも「凝華」を使うことが提案されていました。。
そして、日本の高校でも2022年度から、
気体から固体への変化は「凝華」
と学ぶことになったのです!
大気圧で缶を潰す実験を手軽に
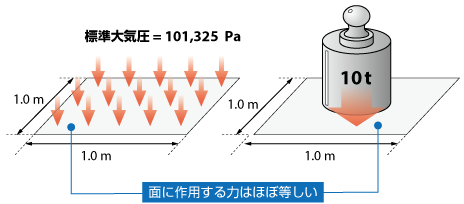
大気圧の大きさは、常圧で1013ヘクトパスカルと教わったと思います。
この大きさをおおよその値で分かりやすく言い替えると、
「1cm2あたり1kg重の力」
又は、
「1辺10cmの正方形の面に100kgの重さ」
となります。
これでだいたい実感できるのではないでしょうか?
幅1m長さ2mのドアに20トンの力ですから、驚くほどの大きさです!
この大気圧の力を実感できる実験を手軽に出来ないでしょうか?
栓のついたアルミ缶を使うと簡単です!
この空き缶に水を入れて、しばらく沸騰させます。(フタは取って!)
缶の座りが悪いので、キッチンのコンロにまず網を置いてその上で加熱するといいでしょう。
軍手を両手にはめておきましょう。
火を止めたら、缶にしっかりとフタをして下さい。
火傷に充分気を付けて!
あとは、缶が冷えると変化が観察できますが、水をかけても、あおいで風を吹き付けてもいいでしょう。
自然に冷えるのを待ってもいいです。
これ以上缶が潰れないのは、缶が潰れる時に出来るしわが穴になってしまうからなんです。
この穴から外気が入り込んできてしまって、減圧状態が保てないんです。
穴さえ開かなければ、缶はもっとペチャンコになるはずなんですね!
16日の地震 東日本大震災と別タイプ
3月16日深夜に福島県沖で発生した最大震度6強の地震は、
東北地方太平洋沖の日本海溝で、
日本列島を乗せた陸側のプレートの下に沈み込む太平洋プレートの内部が震源で、
東日本大震災とは別タイプだった。
気象庁によると、海側から押され続けることで同プレートに歪みが蓄積し、
プレート内の断層が活動して発生した「逆断層型地震」だという。
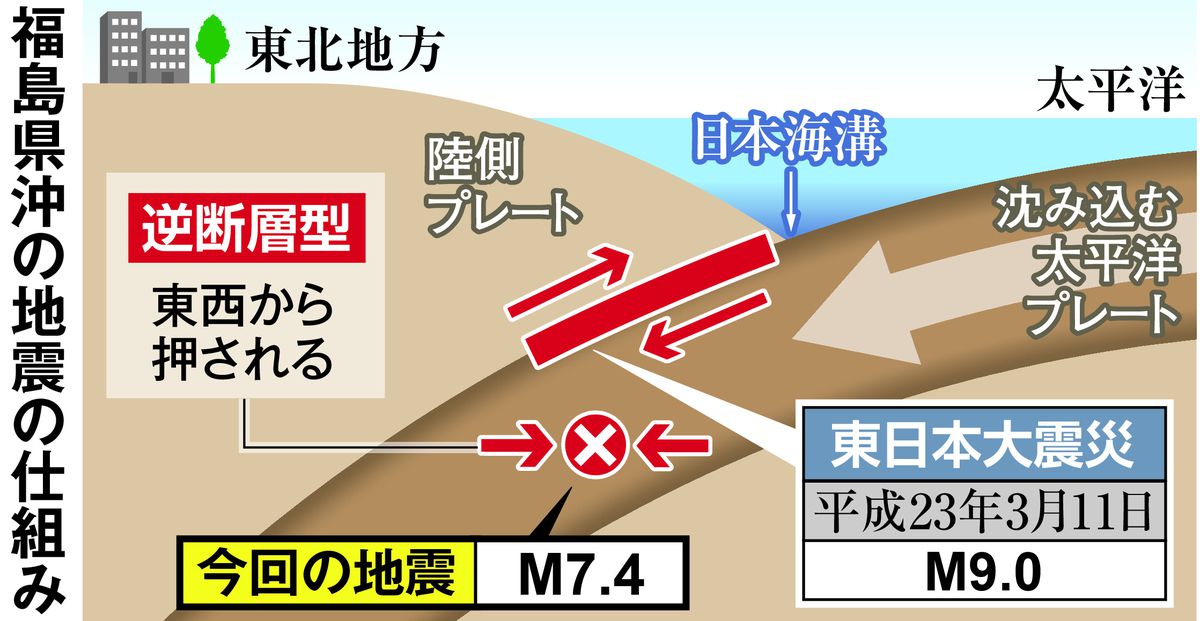
震源が海と陸のプレートの境界よりも下の深さ57キロで、
東日本大震災のようなプレート境界の固着域がすべって起きる「プレート境界型地震」ではないことから、
古村孝志・東京大地震研究所教授は
「発生機構が異なり、東日本大震災の余震ではない」と指摘する。
震源がやや深く、規模もマグニチュード7.4と大きいため、東北から関東にかけて広い地域に大きな揺れが広がった。
発生の2分前に近くでM6.1の地震が起きており、最大震度5弱を記録。
揺れの被害を拡大したとみられる。
古村教授によると、
この付近では、東日本大震災の余震とは無関係に、M7~7.5程度の地震が繰り返し発生してきた。
昨年2月13日にもプレート内が震源のM7.3の地震が発生、最大震度6強を記録した。
一般的に、大きな規模の地震が起きた後は、2、3日のうちに同程度やそれ以上の規模の地震が起きる可能性がある。
気象庁は「揺れが強かった地域は、今後1週間程度は最大震度6強程度の揺れに警戒してほしい」と呼びかけている。
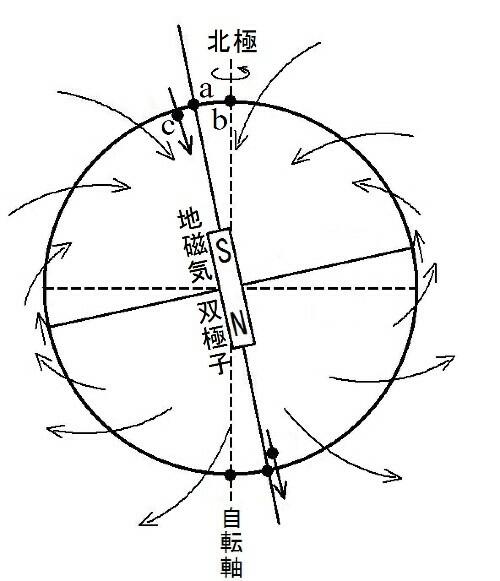
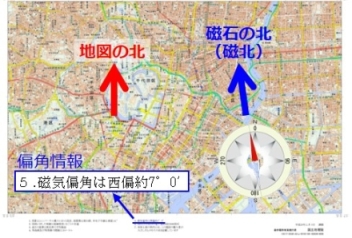
方位磁針の「北」、西にずれる 地磁気の変動影響か
国土地理院は2日、方位磁針が指し示す北(磁北)が5年前に比べ、県庁所在地の平均で西に0.3度ずれたとの調査結果を明らかにした。
地球が持つ磁気(地磁気)が変動しているためと考えられる。
地磁気の極は北極や南極とは異なる位置にあり、磁北は地図上の北と一致しない。
地磁気は地殻の影響も受けるため、場所によってずれは異なる。
こうしたずれを補正するため、地理院は5年ごとに地磁気の分布を示した地図を発表している。
2日に発表された2020年版によると、東京では磁北が地図上の北より7.6度西にずれており、2015年より0.3度大きくなった。
いずれの県庁所在地も2015年と比べて西にずれており、札幌、名古屋、大阪などは0.3度変化していた。
磁北と地図上の北のずれは、登山時など方位磁石で方角を調べる際に把握が必要になる。
スマートフォンやカーナビでは自動的に補正される。
ちっちゃな鏡作り
有機化学のアルデヒドの項では、アルデヒドには還元性があり、この還元性は銀鏡反応やフェーリング液の反応で確認できることを学びます。
この銀鏡反応ですが、全く文字通り試験管の内側に銀がキレイに付着して鏡のようになる反応です!
でも見てるだけじゃツマラナイので、持ち帰れる小さな鏡を作ってしまおう! という実験を先日行いました。
単体金属の銀をガラス面均一に析出させるために、銀アンモニア錯イオンを作っておいてこれにブドウ糖水溶液を混ぜます。
ブドウ糖は3種の異性体の混合物として存在しているんですが、これら異性体のうち1つにアルデヒド基(ホルミル基)があり、このアルデヒド基の還元性によって銀のイオンが銀に還元されて析出するという仕組みです。
錯イオンの形態の銀イオンを使っていますが、基本的な考えは
Ag+ + eー → Ag
ということですね。
ガラス面にキレイに銀を析出させるには、Ag+より[Ag(NH3)2]+が適しているということなんです。
ちなみに銀の電解メッキ工場では、[Ag(CN)2]ーを使うので、この原料である猛毒の青酸カリ(KCN)の話題が出てくる訳です。
さて、鏡づくりですが・・・

キレイな鏡を作るための工夫だと思いますが、塩化スズSnCl2を補助剤として使っています。
スズイオンはSn2+よりSn4+の方が安定なので、SnCl2は還元剤として働きます。
つまりここでのSnCl2はブドウ糖と共に銀イオンを還元していることになります。
ガラスですが、スライドガラスを流用してまずはこのように細工しておきます。
銀がガラス片面だけに析出するようにするためです。
銀アンモニア錯イオン溶液は、硝酸銀溶液にアンモニア水を加えていくだけで作れます。
硝酸銀溶液にアンモニア水を少量加えると酸化銀Ag2Oの褐色沈殿が生じます。
2Ag+ + 2OHー → Ag2O↓ + H2O
このあと、この酸化銀の濁りがちょうど消えるところまでさらにアンモニア水を加えていくと、
銀はすべて銀アンモニア錯イオン[Ag(NH3)2]+ に変化し透明溶液となります。
Ag2O + 4NH3 + H2O → 2[Ag(NH3)2]+ + 2OHー
これ以上アンモニア水を入れると銀鏡反応の感度が落ちるので、入れ過ぎないように注意します。
すみません! この後の途中経過の写真がないんですが、仕上がった鏡はこんな感じになりました。
そしてこれは、自分が慌ててテキトーな操作で使った失敗作!(笑)
これじゃあ全然ダメですね・・・
この実験は原理はシンプルなんですが、随所に「コツ」が必要なんですね!
最後に実験後の片づけでの注意点があります。
この実験では、不安定な雷銀という爆発性の物質が生じやすくなっています!
これを避けるために実験後の廃液は食塩水と混ぜて処理します。
銀イオンが食塩水と混ざることで安定な塩化銀AgClが生じるので、この状態の廃液としてから処理業者に引き取ってもらうようにします。
室内火災発生! CO中毒から命守るには?
一酸化炭素(CO)中毒から命を守るためにはどうすればいいのか。
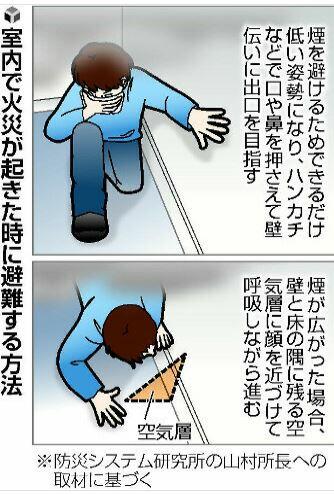
「室内で火災が起きた時は、とにかく低い姿勢になり、出口へと急いでほしい」
火災が発生した室内では、煙が充満する。
視界が遮られるだけでなく、COや炭素の粒子を吸い込むことで呼吸ができなくなる。
このため、出火に気づいた際には煙を避けるため、
できるだけ低い姿勢になり、ハンカチやタオル、衣服などで口や鼻を押さえて壁伝いに避難することが大切だ。
煙が広がった場合は、空気層が残る壁と床の隅に顔を近づけて呼吸しながら逃げることも考える。
COを除去する効果は、ハンカチなどを水でぬらしても期待できないという。
「気道の熱傷を防ぐ効果はあるが、よほど炎に近い場所でなければ意味がない」
「ハンカチをぬらす時間があれば、まずは逃げてほしい」
リチウムイオン電池火災が急増 昨年上回るペース
リチウムイオン電池の発火事故は、民生機だけでなく、さらに信頼性を求められる業務用産業用の機器などでも起きてきました。
最近は改良が重ねられ、発火事故は激減したのではないかと思います。
しかし、活性が極めて強いリチウムを使う電池ですから、元々危険性を持っているということなのです。
枕もとのスマホ、職場に置いてあるモバイルバッテリー、家族に贈ったブルートゥーススピーカー・・・
これらが、夜、留守にしている時、日射を受けて高温になっている時、等々・・・
発火する恐れがないか、いつも気になっているんです。
「取り扱いに気を付けなければならない電池」である、ということを気に留めておくべきだと思います!
最近の、以下の記事を読んでみて下さい。
ここでは、純正以外の規格外の充電器を使って起きた事故が紹介されています。
スマホなど携帯端末に使われるリチウムイオン電池から出火する火災が都内で相次いでいる。
昨年を上回るペースとなっているため、東京消防庁が注意を呼びかけている。
同庁によると、製品別の内訳では、
①モバイルバッテリー20件
②スマホ等携帯電話14件
③コードレス掃除機7件
の順に多かった。
リチウムイオン電池が原因の火災は近年増加している。
5月に都内の住宅であった火災では、リチウムイオン電池を使う電動モップに他社製の充電器を用いたところ出火し、2人がけがをしたという。
東京消防庁は「メーカー指定の純正品を使い、充電中に熱くなるなどの異常があった際は使用をやめてメーカーや販売店に相談してほしい」としている。
電気分解の実験
机上で勉強したことが、実際はどういった変化となって、見たり匂いを嗅いだりして実感することが出来るのか?
こういうことを体験できるのが実験という訳なんですが、実験を行う時は操作も簡単で、実験している人が「あーそうだよな!」と実感出来るやり方を確立させなければいけません。
そこで、実験書やWeb情報など活用して調べるんですが、最終的な現場(実験室)での知恵もすごく重要になると思っています!
現任校の実験についてなんですが、実験方法がとても良く考えられていて、改良も随所に施されていることをいつも実感しているんです!
今回は電気分解の実験を4種類行いましたが、生徒たちにとって結果も分かりやすく実感できたのではないかと思っています。
まずは、塩化銅(Ⅱ)CuCl2 水溶液の電気分解です。
この溶液中では、CuCl2 が Cu2+ と Clー に電離して、これらのイオンが水中を漂っています。
そしてこれらのイオンが各電極に引き寄せられ、次のような反応が起こります。
陽極(+) 2Clー → Cl2 ↑ + 2eー (気体の塩素が発生)
陰極(ー) Cu2+ + 2eー → Cu (金属銅が析出)
こんな感じですね!
これを実感できる実験ですが、下を見て下さい。
この006P乾電池(懐かしい!)を使えばワンタッチで電圧をかけられますし、配線も不要ですね。
また、この細い紙はヨウ化カリウムでんぷん紙という酸化力のある物質を検出する試験紙です。
この実験ならピンセットではなく指先でつまむ操作で充分でしょう。
とても分かりやすい結果が確認出来ていますね!
陰極には赤っぽい金属銅が付着していますし、陽極から発生した塩素ガスの酸化作用によってヨウ化カリウムでんぷん紙が青紫色に変色しています。
塩素ガスは臭いでも確認出来ていましたが、発生した量はごく僅かで問題は起きませんでした。
次は、ヨウ化カリウム KI 水溶液の電気分解です。
この溶液中では、 KI が K+ と Iー に電離してこれらのイオンが水中を漂っています。
陽極(+) 2Iー → I2 + 2eー (固体のヨウ素が析出)
陰極(ー) H2O + 2eー → 2OHー + H2 ↑ (気体の水素が発生)
こんな感じです。
陰極では気体の水素が気泡となっていますし、このあと陰極付近にフェノールフタレイン溶液をたらすと、ピンク色(赤色と覚えて下さい)に変色しOH-の生成が確認出来ます。
一方の陽極では、固体のヨウ素I2が生じたあとすぐに水中のヨウ化物イオンIーと結合してI3-となり、このために褐色となるのです。
I2だけなら濃い紫色が現れるはずですね。
このようなシンプルな実験器具なんですが、炭素棒を固定するセパレーター、試験用の指示薬や溶液を入れたプラスチック製の小容器、時間を測る小さな電子式ストップウォッチなど、毎回の実験で有難さを感じる細かい配慮がなされているんです。
いつも有難うございます!!
異種金属間に生じる電位差の実験
金属は陽イオンになりやすく、金属が陽イオンになる時に電子を押し出します。
金属によってこの電子を押し出す強さが異なるので、2つの異種金属を電解質溶液に浸すと、これら2つの金属電極に電位差が生じることになります。
この電位差が電池の起電力に相当します。
食塩水で湿らせたろ紙の上に、亜鉛Zn、鉄Fe、銅Cu、マグネシウムMg、
の4つの金属を置き、デジタルマルチメーターで電圧を測定する実験を行いました。
デジタルマルチメーターですが、今回使用したのはそれほど高価なものではないそうですが、この実験には性能的に充分なようです。
旧式のアナログ電圧計だと、内部抵抗がそれほど大きくないので電圧が上手く測定できないと思います。
今回の実験での測定値は小数点以下3ケタも表示してありますが、実験方法がややラフだったこともあり、測定値はそれほど正確ではありません。
まあ、おおよその傾向は読み取れたと思います!
コロイドの実験
コロイド粒子は、通常の無機質の分子やイオンの10~1000倍の大きさがあります。
食べ物は、コロイドやコロイドが固まって出来たものがとても多いんです。
牛乳、スープ、ゼリー、豆腐、そしてクリームなんかもコロイドなんですね!
さて、コロイド粒子は大きいのに沈殿せず媒質(水など)中を漂っていられるのは、コロイド粒子が同種の電荷を帯びていて、大きなかたまりにならないからなんです。
無機質のコロイドで見やすく簡単に実験できるのは、水酸化鉄(Ⅲ) Fe(OH)3を使ったものでしょう。
沸騰水に塩化鉄(Ⅲ) FeCl3 水溶液を少量たらすだけで 赤褐色のFe(OH)3コロイドが生成します。
これをセロハンチューブの中に入れて、セロハンチューブごと水中に浸したものが下の写真です。
セロハンはポリ袋(ポリエチレン製の袋)と違って小さなすき間が無数に存在しています。
このセロハンのような膜を半透膜と呼んでいます。
コロイド粒子はこのような半透膜の小さなすき間をくぐり抜けられません。
ですから、水やイオンなどの粒子はセロハンのすき間を通過できますが、コロイド粒子はセロハンチューブの外側に出ていけないんです。
これを利用した上の写真のような操作を透析と呼び、コロイドの精製などに使われます。
人体内の腎臓でもこれと同様のことが行われていて、血液中の老廃物だけが腎臓内の半透膜を通って尿として体外に排出されるようになっているんです。
腎臓の機能が著しく低下してしまった時に行われる人工透析では、体外に血液を導いて人工腎臓装置に透析を行わせている訳ですね!
タングステンという金属
タングステンと言えば、白熱電球のフィラメントの素材として教わったのではないかと思います。
フィラメントに電流が流れると、ジュール熱が発生しフィラメントが高温になって眩い光を放つ訳です。
ですから、「タングステンは高温に耐える融点が非常に高い金属」ということなんですが、他の物性はどうなのか?
昨日、突然タングステンのインゴットを見て触れる機会があったんです!
この純粋なタングステンのインゴットは、1辺が2.5cmの立方体です。
すると体積は、(2.5cm)3 ≒ 15.6cm3 ですね。
そして、持ってみて凄くビックリしたんですが、ずっしりと重いんです!
実際の重さはどれくらいあると思いますか?
では、重さを量ってみましょう!
ちょっとビックリしました!
293.3gですよ!!
最初ケタを見間違えているのかと思いました。(29.33gじゃあ軽すぎですが)
密度を計算してみましょう!
293.3g/15.6cm3 ≒ 18.8g/cm3 となりました!
(正確な公表値は19.3です)
他の身近な金属の密度ですが、
鉄が7.9、鉛が11.3ですから、タングステンの19.3はかなり大きな値だと言えます。
実際に手で持ってみると、その重さにビックリすると思います!
もし興味があれば、是非実際に手で持ってみて重さを肌で感じてみて欲しいんです。
セッケンを自作する時に考えること
勤務校の授業でセッケンを作る実験を行いました。
セッケン作りは久しぶりでしたが、牛脂(ヘット)、ヤシ油(ココナッツオイル)、ヒマシ油の混合油脂に水酸化ナトリウムを反応させる一般的な方法で作りました。
上の2つの液体には色が付いていて、色も違います。
これは、出来たセッケン素地に糖を入れ温度を上げ、糖を少しだけ焦がすことで色を付けています。
色が濃い方はブドウ糖を使っています。
この2つのセッケンを容器に2段重ねになるように流し入れて、プリンのようなセッケンに仕上げています。
面白いでしょう?
このようにセッケンは割と簡単に作れるんですが、品質のいいセッケンを作ろうとするとちょっと難しいんです。
セッケンを作る時の反応は、
油脂 + 水酸化ナトリウム → 高級脂肪酸ナトリウム + グリセリン
のように進み、「高級脂肪酸ナトリウム」がセッケンの本体です。
同時に生じるグリセリンは、肌触りを良くする効果も期待出来るので取り除かない方がいいでしょう。
さて、この反応で、油脂が過剰だと生成物には油脂が含まれ脂っぽいセッケンになるので良くないですね。
また、水酸化ナトリウムが過剰だと生成物に残った水酸化ナトリウムが含まれてしまい、人体には使えないセッケンになってしまいます!
しかし、どちらの原料も反応に過不足なく計量するのは簡単ではないし、適量混合出来たとしても混合物質は100%反応せずにごく少量残ってしまうようなんです。
上の写真を見ると、出来た液体は薄い褐色の均一な透明溶液になるので、反応は完結しているように見えるんですが・・・
そこで、ずっと考えてきたのは、
この反応(けん化)を起こすために、水酸化ナトリウムではなく、炭酸ナトリウムが使えないかということです。
炭酸ナトリウムなら過剰に使って残ったとしても、人体への影響が少ないでしょうから。
以前、炭酸水素ナトリウムを使って2晩ほどかけて反応させるよう試みたんですが、全く反応しませんでした。
このけん化反応を開始させるには水酸化物イオンOH-が重要な働きをします。
炭酸水素ナトリウムの加水分解によって生じるOH-は非常に少ないので(塩基性がごく弱いので)、より塩基性の強い炭酸ナトリウム水溶液なら上手くいくのではないかという見通しです。
元々セッケンは、肉の脂身に灰(炭酸カリウムが含まれる)が降りかかって偶然に発見されたと言われています。
また、ケイ酸ナトリウムを使って作る例も紹介されています。
ですから、油脂と炭酸ナトリウムでも上手く行きそうだと思っているんです。
でもネット検索してみると、灰でセッケンを作る例は見つかるんですが、炭酸ナトリウムで作る例は見つかりません・・・
ちょっと挑戦してみようと思っているんです!
残念ながら見れませんでした・・・皆既月食
月の出から気にしていて、南東の空を見上げていましたが、さっぱり何も見えません。
20時10分から屋根に上ってみましたが、どこにも月が見えない!
高度が低くて我が家からは見えないのかも? と思っていたら、信号灯を点滅させながら飛んでいる飛行機が見えないんです。
思ったより雲が出ていたんですね・・・
どうしようもないので、家の中に入ってYoutubeの北海道なよろ市立天文台きたすばるライブカメラの配信を見ました。
https://www.youtube.com/watch?v=ifhz3GO_Qs8
全国的に厳しい観測だったようなので、これが参考になりますね!
あと、沖縄では、赤銅色の変化が見られたようです。
我が家の屋上からは、20時59分のこの写真が精いっぱいでした!
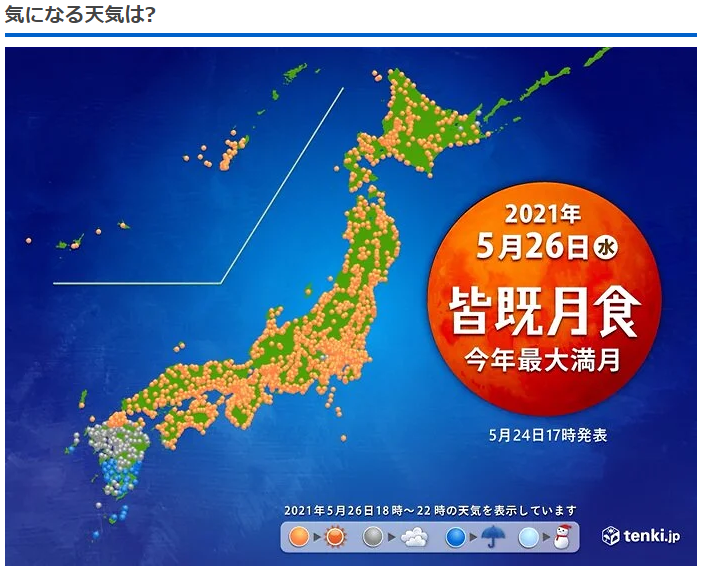
26日(水曜) 今年最大の満月「スーパームーン」で皆既月食
26日水曜の夜、のぼってくる月は、満月です。
この日の満月は、特徴が2つあります。
1つは、皆既月食が起こるということです。
皆既月食は、月が赤銅色と呼ばれる、赤黒い色に見えて、今回の皆既月食は、天気の条件さえ良ければ、全国で観察することができます!
国立天文台によりますと、月は18時44分ごろから欠け始め、
皆既食の始まりは20時9分ごろ、
皆既食の最大は20時18分ごろ、
皆既食の終わりは20時28分ごろ、
欠けた部分が小さくなっていって、部分食が終わるのは21時52分ごろです。

もう1つは、26日水曜の満月は、2021年では地球に最も近い満月でもあります。
そのため、最も大きく見えることから「スーパームーン」とも呼ばれるのです。
地球に「最も近い満月」は、「最も遠い満月(12月19日)」に比べて、視直径が約14%大きく、約30%明るく見えます!

さて、26日水曜夜の天気は?
沖縄と、中国、四国から北海道は、広い範囲で晴れそうです!
「皆既月食」&「今年最大の満月」を観察するには、最適の天気でしょう!
ただ、晴れる夜は、気温がどんどん下がります。
貴重な満月を眺める時には、しっかり上着を着て、楽しんでください!
100平方センチメートルの面積にかかる大気圧による力は?
以前、「1辺10センチの正方形にかかる大気圧による力の大きさはどれくらいか?」
と問題にしましたが、その解説を書きたいと思います。(遅くなってすみません)
まず大気圧の大きさですが、1013hPa(ヘクトパスカル)と覚えていると思います。
ここでのh(ヘクト)は単位の接頭辞で、100を表しています。
すると、
1013hPa = 101300Pa
これは約100000Pa(10万パスカル)
となりますね。
また、1Pa(パスカル)の定義ですが、1m2の面積に1N(ニュートン)の力が加わる大きさの圧力となっています。
さて、1kgの質量の物体にかかる重力の大きさ(つまり重さ)を考えてみます。
W = mg = 1kg × 9.8m/s2= 9.8kg・m/s2=9.8N ≒ 10N
となるので、
1kg重 ≒ 10N
ということは、
1N ≒ 0.1kg重
となります。
ですから、こう覚えておくといいと思います!
「1Paとは、1平方メートルに約100グラム分の重さがかかる圧力」
そして、大気圧1013hPaは、
「1平方メートルに約1万キログラム分の重さがかかる圧力」
となりますね!
次は、1辺10cmの正方形の面積をm2単位で求めてみましょう。
10cm=0.1m
ですから
(10cm)2=(0.1m)2
よって
100cm2=0.01m2
となります。
さあ、最後の答えを出してみましょう!
1辺10センチの正方形にかかる大気圧による力の大きさは?
100000Pa × 0.01m2 =1000N
そして、この1000Nは、約100kg重となります!
「1辺10センチの正方形にかかる大気圧による力の大きさは約100kg重!」
ちょっと信じられない重さだと感じませんか?
そして1平方メートルには、この100倍の10000kg重つまり10トン重の重さが加わっていることになるんですね!
結露で校舎内の床が広範囲に濡れる
今朝の校舎内の床、特に廊下の床面は結露のため広範囲に濡れていました。
校舎内の、特にコンクリートにリノリウムを貼った「冷たい床」は全て濡れているような状況でした。
この現象はそれほど頻繁に発生する訳ではないんですが、ちょうど今頃発生しやすいと思います。
外気温が上がってきているんだけど、校舎全体はまだ温まっていなくて壁や床は冷たいくらいの時期ですね。
そんな時期に、雨が降るような蒸し暑い大気が校舎内に入ってくると、大気中の水蒸気が校舎内の冷たい所で結露します。
今日気付いたと思いますが、床だけでなく壁や金属製の手すり、窓枠なんかも濡れていたと思います。
湿度の高い大気が入ってきても、校舎の温度が低くなければ結露は起こらないんですね。
校舎のようなコンクリート製の建物は比熱が大きく、すぐに温まったりすぐに冷えたりしにくいんです。
ということで、急に外気温が上がってその大気の湿度が高い時にこの現象は発生する訳です。
でも、校舎の窓や入口が開いていない時は、気密性が割と高い校舎の中に大気は入っていきません。
登校時校舎の入り口が大きく解放されて、暑いからとたくさんの窓も開けられると一気にこの結露が起こる訳ですね。
梅雨時期でなくても、台風が生ぬるい湿った空気を持ってくる時にも同じようなことが起こります。
台風の時は風が強いので、ドアや窓を閉め切っていても隙間から大気が入り込んできて結露が起きるんです。
今度同じようなことに遭遇したら、良く観察してみて下さい。
床が濡れているのは、外の雨が入り込んできたからではないんですね。
さて今日このような状況で、校舎内で滑りそうになりませんでしたか?
上履きはスリップに対して強くはないと思うので、充分に気を付けて下さい!
スリップして転倒すると大ケガになることもありますから!
シンプルだけど良く考えられた実験(詳細)
前回ざっと書いたこの実験について、原理も含めて記録しておきたいと思います。
フラスコ内の水をしばらくの間沸騰させると、水蒸気が発生しフラスコ内の空気は追い出され水蒸気だけになります。
火を止め、フラスコにピペット(俗称スポイト)を刺したゴム栓をはめ込むのですが、このゴム栓はこんな感じに作ってあります。
これをフラスコにこんな感じにセットします。
フラスコ内の温度が下がっていくと、内部の水蒸気は凝縮して液体の水になっていくので、フラスコ内部の気圧が下がっていくことになります。(フラスコ内の気体分子が減っていくから)
するとフラスコ内は100℃を下回っているにもかかわらず水が沸騰することになるんですが、これを減圧沸騰と呼んでいます。
フラスコ内の湯から泡が出ていて沸騰している様子が分かるでしょう?
フラスコの内部がいつも水面を押さえつけていた大気圧より低い圧力となるため、100℃を下回る温度でも沸騰できるようになるという訳です。
「高い山の山頂では気圧が低く、100℃にならずにお湯が沸騰する」と聞いたことがあると思いますが、これと同じ理由です。
ちなみに圧力なべはこの逆で、なべに閉じ込めた水蒸気でなべの内部が高圧になるようにしてあるんです。
こうすると100℃を超えないと水が沸騰出来ないことになり、100℃を超える温度で調理が出来ることになる訳ですね。
さて、減圧沸騰がしばらく続くと水蒸気が新たに生じるためフラスコ内部の圧力は上昇していきますよね。
すると沸騰が収まっていく訳ですが、フラスコと中の湯は外気にさらされ続けているので冷えていく一方です。
下の2つの写真では、水蒸気の凝縮がより多く起こってきてフラスコ内に水滴が沢山付着してきている状況が分かると思います。
さあ、生じた水蒸気が冷えてまたまた減圧沸騰が起こるより早くフラスコ全体が冷えるとどうなるでしょうか?
フラスコ内部の水蒸気が急激に凝縮すると、内部の圧力も急激に減少します。
ここでピペットのゴム球に着目して下さい!
ゴム球の内部は外の大気に通じているのでゴム球内部は大気圧によって外側に押され続けています。
ここでフラスコ内部つまりゴム球外部の圧力がすごく小さくなったらどうなるでしょう?
ゴム球は内側から押されている力で大きく膨らむことになりますよね?!
ごらんの通り、すごく見栄えのするはっきりとした結果になりました!
この実験はやってみた後で気付いたんですが、とても良く考えられているんですね!
まず、ピペットのゴム球の代わりに普通のゴム風船で実験する例があるんですが、風船は軟弱なのですぐ膨らんでしまって減圧沸騰がしっかりと見られないのではないかと思います。
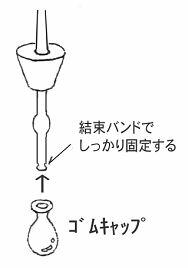
そして、ピペットのゴム球に隙間なく接続できるのはガラスピペットの本体ですよね?
さらに、ピペット本体とゴム球の接続を確実にするために結束バンドを使っていることも良く考えたと思います!
さて、この実験の全体像と原理は見えたでしょうか?
最後に問いを1つ書いておきたいと思います。
1辺10センチの正方形つまり100cm2の面積にかかる大気圧による力はどれくらいだと思いますか?
答えは次回に!
シンプルだけど良く考えられた実験
まずフラスコ内の水を沸騰させます。
火を止め、ピペットを付けたゴム栓をはめます。
放置して冷やすと、少し間をおいて減圧沸騰が始まります。
そして、さらにフラスコを冷やすと、最終的には・・・
さて、こうなる理由は・・・?
CO2排出削減の救世主的技術、二酸化炭素そのものを回収する方法!
すでに大気中に排出されてしまった二酸化炭素CO2、あるいは、これからもまだ排出されるであろうCO2そのものを、どのように除去したらいいのでしょうか?
その最先端技術の紹介です。
自然界における二酸化炭素循環
人類が化石燃料を使う前、地球上においてCO2は基本的に水や酸素と同様に、増えもせず減りもせず、うまく循環していたはずです。
地球化学的循環は数百万年オーダーの変動で、大気中のCO2は水に溶け、やがて炭酸カルシウム(CaCO3)となって固体になり、火山の爆発によりCO2が大気中に出て、また水に吸収されるという循環サイクルが完成します。
生物学的循環は数万年オーダーの変動で、植物は大気中のCO2と水から光合成によりデンプンやセルロースを生成。
この時に酸素が発生し、動物は酸素を吸ってCO2を吐いています。このように、CO2や酸素はバランスよく循環しています。
これが自然の摂理です。
さて、人為的CO2排出ですが、人類最初の化学反応は火を使った燃焼でした。
人類は、火を使って木や草を燃焼させエネルギーを獲得してきました。
木や草は炭素を骨格とした有機化合物からできていますので、燃やせばCO2が発生します。
この燃焼という化学反応は現在でも行われており、重要なエネルギー獲得手段になっているのは周知の通りです。
そして人類は、有機化合物からできている石炭・石油・天然ガスといった化石燃料を大量に燃やし、地球化学的循環や生物学的循環に比べて微々たる短期間、過去200年の間に、一方的に大量のCO2を排出してきました。
この人為的に排出されたCO2はリサイクルされておらず、CO2は大気中に溜まる一方です。
では、CO2はどのように削減すればいいのでしょうか。
二酸化炭素そのものを直接回収するには
今注目を集めているのは、化石燃料をできるだけ使わない、あるいは再生エネルギーの活用などの間接的削減といったことではなく、CO2そのものを直接回収して削減する技術です!
この技術は、ダイレクトエアキャプチャー(DAC)と呼ばれますが、経済や社会活動に制約を与えることなく、CO2だけを削減することができる温室効果ガス削減の救世主的方法と言えるでしょう。
以下、いくつかの研究・開発例を紹介します。
<神戸学院大学・稲垣教授考案>
アンモニア(NH3)など窒素原子を含む化合物であるアミン類がCO2を吸収することは周知の事実ですが、一緒に水を吸収してしまう欠点がありました。
しかし最近、メタキシリレンジアミンを用いると、この欠点を克服できることが見出されました。
吸収されたCO2を取り出すためには一般的には高温が必要ですが、この場合にはCO2吸収後、比較的低温の120℃でCO2を放出しますので、早期の実用化が望まれます。
<公益財団法人 地球環境産業技術研究機構考案>
CO2を吸収する化学吸収液(2ーイソプロピルアミノエタノール水溶液にピペラジン誘導体やエタノールアミン誘導体を含むもの)や、固体吸収材(多孔質のシリカゲルにアミンを担持させたもの)を開発しています。
こうしたCO2を化学的に吸収する方法の開発は重要です。
<日本CCS調査株式会社考案>
現在、日本CCS(Carbon dioxide Capture and Storage)調査が、苫小牧沖の海底1000m以上の深さにある隙間の多い砂岩などからできている貯留層に、製油所から排出されるCO2を大気放出前に回収(活性アミンプロセス)して貯留する実証プラントを稼働させています。
かなり大掛かりな施設ですが、こちらも実用化が期待されます。
<JFEエンジニアリング株式会社考案>
清掃工場から排出される排ガスからCO2を回収して利用するCCU(Carbon Capture and Utilization、二酸化炭素回収利用)プロセスの実証実験を開始すると発表しました。
このプラントのCO2吸収方法も、天然ガスプラント建設等で実績のあるアミン吸収法です。
CO2回収を清掃工場に適用すると、ごみに含まれるバイオマス分を合わせた「ネガティブカーボン(CO2回収量>排出量)」を達成することが可能になります。
<日揮株式会社考案>
セラミック製のゼオライト膜を活用したCO2分離・回収技術の実証試験を米国テキサス州で開始しています。
日本ガイシと共同開発したゼオライト膜は1ナノメートル以下の微細な穴を多く持つのが特長で、ちょうどCO2を通す大きさなので、原油生産時に出てくるメタンなど他のガスから分離することができます。
抗菌シート・ワサオーロ
職場でお弁当が出る日が1年に数回あるんですが、ある日のお弁当を開けてみると、何やら文字の書いてあるプラスチック製フィルムが蓋のように置いてありました。
この写真の背景はグレーですが、薄い透明なシートに白字で印刷がしてありました。
ワサオーロ?
「ーロ」の所は読み方があるのでしょうか?
この5文字で登録商標(TM)になっているようですから、何か意味が込められているんだと思います。
ネット上で調べてみたら、次のようなことが書いてありました。
天然素材を使った抗菌シートなんですね!
三菱ケミカルフーズ株式会社は、食品向け抗菌・鮮度保持シート『ワサオーロ』を開発しました。
ワサオーロは、ワサビやカラシの辛味主成分であるアリルカラシ油(アリルイソチオシアネート)を主剤とした抗菌・鮮度保持シートです。
消費期限の短いお弁当やお持ち帰り食品の品質保持適しています。
菌やカビ・酵母の増殖を抑える特性があり、食品にシートをかぶせて蓋をすることで、速やかに抗菌効果を発揮します。
グレタさん痛烈批判「各国が掲げるのは架空の目標」
スウェーデンの環境活動家グレタ・トゥンベリさんは、世界のリーダーが参加するオンラインの会合で、各国の気候変動問題への取り組みについて「架空の目標」を掲げていると痛烈に批判しました。

「世界中のリーダーは気候の緊急事態といいますが、危機の中、すぐに行動する代わりに、彼らは漠然として不十分で架空の目標を掲げています」
世界の政財界のリーダーが参加する「ダボス会議」の主催者がオンラインで開いた会合で、グレタさんは日本を含め各国が掲げる2050年までに温室効果ガスの排出量を実質ゼロとする目標について、「漠然として不十分で架空」だと指摘。
「夜中、家が燃えているのに、10年、20年、30年後に消防署に電話するようなものだ」と厳しく批判しました。
さらに「国民の意識が低いために、リーダーたちはほとんど何からも逃げることが出来る」として、この問題に関心を持つよう広く呼びかけています。
カーボンリサイクルで二酸化炭素を燃料に?!
「カーボンリサイクル」と聞けば、炭素の再利用だろうと考えます。
人間が利用しているエネルギーの大部分は、石油などの化石燃料を燃やすことで得ています。
「カーボンリサイクル」とは、その結果で生じる二酸化炭素を再利用する技術ですね。
そのリサイクルのうち、「プラスチックのような炭素化合物の原料に二酸化炭素を使う」といったようなことは可能なんだろうなと思います。
ところが、「エネルギーを放出して出来た二酸化炭素を燃料に利用する」と聞けば、ちょっと信じられない驚きを感じます!
でも良く考えてみれば、植物にはそれが出来ているんですよね!
光合成による炭酸同化作用です。
二酸化炭素と水から、酸素と炭水化物を生産している訳ですが、光エネルギーを得ながらこの反応を起こしています。
この結果、生じた炭水化物は光からのエネルギーを蓄えたもの、つまり燃料として利用できるものとして出来上がっている訳です!
人工的にこの光合成を真似することが未だに出来ない訳ですが、このような反応が他にもあるのではないだろうか・・・
地球温暖化の原因になっているといわれるCO2の排出量を減らすことは、今やグローバルな課題になっています。
エネルギー分野においては、CO2排出量の少ないエネルギー資源への転換をはかること、省エネルギーに努めることなどが大切です。
加えて、CO2を分離・回収して地中に貯留する「CCS」、分離・回収したCO2を利用する「CCU」も、大気中のCO2を削減するための重要な手法として研究が進められています。
このようなCO2の利用をさらに促進するべく、研究開発をイノベーションにより進めようという取り組みが、「カーボンリサイクル」です。
CCUでこれまで一般的だったのは、「EOR(原油増進回収技術)」と呼ばれる手法への利用です。
たとえば、油田にある原油をできるだけ回収するためには、水などを、圧力をかけて注入し、岩石の小さな穴などに溜まっている原油を押し流します。この時、水の代わりに炭酸ガスを圧入するのが、CO2を使ったEORです。
もうひとつ、現在一般的なCO2の利用先としては、ドライアイスや溶接などに直接利用する方法があります。
しかし、こうした方法だけでは、利用されるCO2の量は限られてしまいます。
そこで、CO2を“資源”ととらえ、素材や燃料に再利用することで大気中へのCO2排出を抑制する、そのために世界の産学官連携のもとで研究開発をおこないイノベーションを進めていこうとする取り組みが、経済産業省が提唱する「カーボンリサイクル」です。
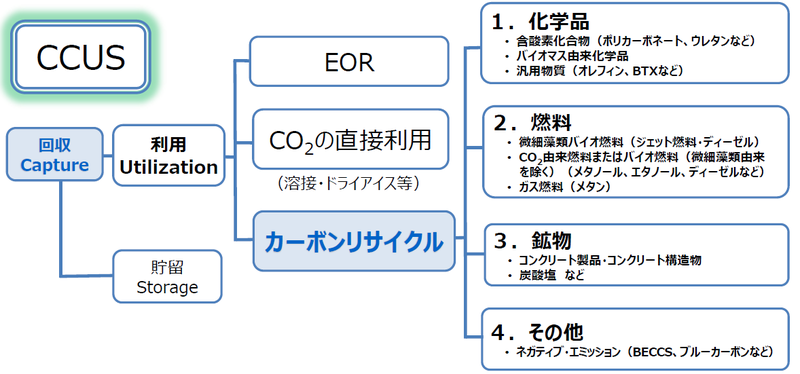
CO2の利用先としては、①化学品、②燃料、③鉱物、④その他が想定されています。
①化学品では、具体的には、ウレタンや、プラスチックの一種でCDなどにも使われるポリカーボネートといった「含酸素化合物」が考えられています。
また、バイオマス由来の化学品や、汎用的な物質であるポリプロピレンやポリエチレンなどの樹脂も利用先となりえます。
②燃料では、光合成をおこなう小さな生き物「微細藻類」を使ったバイオ燃料や、バイオマス由来のバイオ燃料がCO2の利用先として考えられています。
③鉱物では、「コンクリート製品」や「コンクリート構造物」が考えられています。
具体的には、コンクリート製品などを製造する際に、その内部にCO2を吸収させるものなどです。
④その他として、バイオマス燃料とCCSを組み合わせる「BECCS」、海の海藻や海草がCO2を取り入れることで海域にCO2が貯留する「ブルーカーボン」などが考えられています。
これらは総称して「ネガティブ・エミッション」と呼ばれます。
新型コロナウィルス等の殺菌用LEDを開発、量産へ
発光ダイオ―ド(LED)製造大手の日亜化学工業は、LEDで紫外線を照射して新型コロナウイルスを不活化して殺菌にも利用できる装置を開発したと発表した。
空気清浄機やエアコンなど家電の内部に取り付けたり、紙類などの消毒に活用できたりする可能性がある。
ただし、人体への影響を考慮すると、肌に直接照射することは困難という。
二酸化炭素は「無毒」と教わりますが、実は怖い中毒も!
昨日12月22日午前、名古屋市のホテル地下駐車場で、充満した煙を吸うなどして、作業員と周辺の方11人が病院に搬送され、このうち50代の男性作業員が死亡しました。
二酸化炭素を発生させる消火設備が作動し、煙が充満したとみられています。
この消火設備は二酸化炭素を注入することで酸素の濃度を16%以下にし火を消す仕組みです。
二酸化炭素の消火設備は、スプリンクラーで水をかけられない、主にコンピューターなど電気設備のある場所で使われていて、火災報知機と連動して自動で動くものもあるといいます。
一方、二酸化炭素は人体に悪影響を及ぼす可能性があるため、最近は窒素などで代用されることが多いといいます。
この事件では、不幸なことに犠牲になられた方が出てしまいました。
そして、この報道中にもある「酸欠とは別の二酸化炭素の有害性」について、過去の事故を思い出したので記しておこうと思います。
1997年7月12日夜、青森県八甲田山のくぼ地で、訓練中の自衛隊員3人が死亡する事故が起きた。
死因は、火山性の二酸化炭素ガスと見られている。
コーラやビールの気泡やドライアイスなど、身近な存在でもある二酸化炭素。
実は、人間や動物をあっという間に倒す怖い一面を持っている。
しかし、毒性の仕組みはまだ良く分かっていない。
どんな条件の時、二酸化炭素の中毒は起きるのか。
事故の翌日、現地のガス成分を調べた報告書によると、くぼ地での二酸化炭素濃度は15~20%だった。
大気中の二酸化炭素濃度は約0.03%なので、このくぼ地では、通常の約500倍もの濃度があったことになる。
二酸化炭素が原因だとすると、自衛隊員らが倒れたのは酸素が欠乏したせいか?
それとも高濃度の二酸化炭素そのもののせいだろうか?
命にかかわる酸素欠乏は、空気中の酸素濃度が12%を下回った時と言われている。
二酸化炭素濃度が20%の時の酸素濃度は16.7%で、致命的な酸欠状態とは言えない。
一方、一般的に二酸化炭素を30分間吸い続けても後遺症がない「脱出限界濃度」は5%とされている。
10%の二酸化炭素を吸うと、耳鳴りやふるえが起き、1分間で意識を失う。
30%になると、即座に意識不明の状態になる。
酸素20%、二酸化炭素80%の気体を犬に吸わせたら、1分で呼吸が止まり、数分で死亡したという報告があるという。
この実験は、大気と同じ濃度の酸素(大気の酸素濃度は約20%)があっても、二酸化炭素が一定量以上あれば、中毒を起こすことを示している。
1986年8月、西アフリカ・カメルーンでは、湖から火山性の二酸化炭素ガスが大量に噴出、湖の近くで、村人約1200人のほぼ全員が死亡する事故が起きている。
火山性ガス以外では、車でドライアイス運搬中にドライアイスが気化して中毒を起こした例や、二酸化炭素消火装置による例などがある。
ドライアイス2キログラムは、室温だと1時間で約350グラムが気化して約200リットルの二酸化炭素になる。
車内空間が約2立方メートルの軽自動車の場合、濃度は約10%になり、密室状態にしておくと中毒を起こす条件になる。
ドライアイス販売会社は「車で持ち帰るお客さんには、窓を開けて運転するよう呼びかけています」と言う。
二酸化炭素ガスにすばやく意識を奪う作用があることは、18世紀にはすでに分かっていたが、なぜそのような効果があるのか、仕組みはいまだに解明されていない。
大阪大学医学部麻酔学の吉矢生人教授は「二酸化炭素ガス以外にも、笑気ガスやエーテルなど麻酔効果を持つ気体はいろいろありますが、肺から吸入して脳に作用するメカニズムは、どれもわかっていません」という。
<呼吸や飲み物、また人工呼吸での二酸化炭素の心配は?>
人間は、呼吸で酸素を取り込み、二酸化炭素を放出している。
呼気中に含まれる二酸化炭素は約4%なので、口移しで空気を送り込む人工呼吸では、二酸化炭素中毒を起こす心配はない。
炭酸飲料やビールの泡に含まれる二酸化炭素は、肺でなく胃に入る。
胃酸で気体になり、ゲップとして排出されるので、こちらも中毒の心配はない。
(注)大学入試「化学」の中での知識では
二酸化炭素は常温では気体で、その性質は、
「無色」「無臭」「無毒」「水に少し溶ける」です。
アンモニア合成の発明者ハーバー 「栄光と影」(2)
ベルギー西部のイーペルは、第一次世界大戦中の1915年4月、史上初めて本格的な毒ガス戦の舞台の町となりました。
催涙ガス弾などはそれまでにも使われていましたが、ドイツ軍はイーペルの草原で4月22日、致死性の高い大量殺傷用ガスを初めて用いたのです。
人の粘膜を破壊し、呼吸困難などに陥れて殺害する塩素ガスです。
これをきっかけに、ドイツ軍に限らず英仏など連合国側もたがが外れたように化学兵器を使い始めました。
双方はホスゲンなど新種の兵器を次々に投入。
第一次大戦での毒ガスによる死者は約10万人に上り、市民も含む100万人以上が負傷したといわれています。
戦争と科学の発展は切っても切れないのですが、その陰で戦闘員ではない大量の一般市民が命を落としてきました。
こうした兵器を開発した人は、どんな思いで生涯を過ごしたのでしょうか。
「平時は人類のため、戦時は祖国のため」
この塩素ガスを兵器として開発したのが、「化学兵器の父」と呼ばれるドイツの化学者フリッツ・ハーバー博士(1868~1934)だったのです。
「科学というものは、平時は人類のため。戦時は祖国のため」
それが愛国者だった彼のモットーでした。
開発に成功した時、ドイツ国内ではほとんど反対の声もなく、彼はまさに英雄でした。
彼はドイツのエリート層、特にドイツの皇帝に認められたい一心だったのです。
第一次大戦が終わった年の1918年には、過去に手掛けたアンモニア合成法の業績が認められてノーベル化学賞まで受賞しています。
もっともこの受賞には戦時中の敵国だった英国やフランスから激しい非難の声が上がりました。
ですが、ハーバーの名声はノーベル賞を機にさらに高まっていきました。
今も続く追悼式
イーペルは毒ガス戦だけでなく激しい砲撃戦の舞台ともなりました。
今、この町には当時ドイツと戦った英国側の戦没兵の名前が刻まれた門「メニン・ゲート」があります。
大英帝国戦没者墓地委員会が1927年に建立したもので、54896人の名が残っています。
英国をはじめとした連合軍兵士は、この門を起点に戦場へ向かいました。
門にはオーストラリアやインド、カナダなどからの出征兵士の名前も多く刻まれています。
祖先の追悼のため、今も世界中から多くの人々が訪れる場所なのです。
イーペルでは毎晩、戦没者の追悼演奏が行われています。
式典を主催する民間団体「ラストポスト協会」はトランペット演奏をする楽団を含め、20人以上のスタッフ全員がボランティア。
各自、仕事が終わってから門に駆け付け、15分ほどの式典を行います。
この団体幹部のベノワ・モトリーさんによると、
「1928年以降、ナチス・ドイツによる占領時代を除いて毎日続けています。追悼の思いを一日たりとも忘れないためです」
2020年には新型コロナウイルスの影響でこのイベントの続行が危ぶまれました。
ですが欧州メディアによると、今も見物客の人数を制限し、互いの距離を取りながら、追悼演奏は続けられているということです。
「英雄」を待ち受けていた運命
さて、ドイツの英雄となったハーバーはその後どうなったのか。
1933年にヒトラー率いるナチスが政権を握ると、彼の人生は暗転していく。
彼はユダヤ人だったのだ。
ナチスのユダヤ人迫害政策の影響で、徐々にハーバーは「追われる身」となる。
ドイツを愛し、ユダヤ教からキリスト教に改宗までしたハーバー。
だが彼は結局そのドイツから裏切られ、1933年に研究機関を去ることになる。
フランスに住んでいた息子を頼り、まずハーバーはパリに逃げた。
さらに英国などを転々とした後、1934年1月にスイス・バーゼルで病死した。
ライン川が流れるこの町の目と鼻の先には、彼が愛し抜いた祖国ドイツがあった。
世界はその後も化学兵器を使い続けた。
第二次大戦、ベトナム戦争、イラクのクルド人が虐殺されたハラブジャ事件、化学テロである地下鉄サリン事件、そしてシリア内戦。
第一次大戦から100年以上たった今も、それは現在進行形で人類の脅威であり続けている。
シリアではアサド政権による猛毒神経ガス・サリンなどを使った化学兵器攻撃が何度も疑われている。
だが政権側はその度に使用を否定し、国際調査も進まない。
ハーバーは毒ガスの使用について、同僚にこう説明していたという。
「むしろ使用によって戦争を早く終結させ、多くの人の命を救える」
この論理は、のちに第二次大戦で広島、長崎への原爆投下を正当化した米国側の主張にそっくりだ。
しかし大量破壊兵器の使用はこうして21世紀の今も続き、多くの人が命を失い続けているのが現実でもある。
祖国ドイツのため、化学兵器開発を誇りに思っていたハーバー。
だが彼は死の直前、息子にこんな遺言を残している。
「クララと一緒の墓に埋めてほしい」
毒ガスを開発した男が人生の最後に思い出したのは、その毒ガスの使用に抵抗した最初の妻クララだったのだ。
二人は今、スイス・バーゼルの同じ墓に眠っている。
アンモニア合成の発明者ハーバー 「栄光と影」(1)
今日、ドイツの化学者フリッツ・ハーバーについての記事が目に留まりました。
高校の化学の教科書に必ず登場するハーバーですが、自分の知らなかった一面を初めて知り、大きなショックを受けました。
ノーベル賞も受賞した彼の栄光と影について記しておこうと思います。
化学の教科書の、「化学平衡」「非金属元素窒素」の項に必ず登場するのが、アンモニアの工業的製法「ハーバー・ボッシュ法」です。
このアンモニアの合成法は、ドイツのフリッツ・ハーバーが発明し、カール・ボッシュが触媒を改良して工業化に成功させました。(1906年)
当時、このアンモニア合成法は、「水と石炭と空気からパンを作る方法」とも言われた大発明でした。
このように言われた理由ですが、パンの原料である小麦を始めとして農作物を育てるには窒素分を含む肥料の十分な供給が不可欠です。
その窒素を供給する化学肥料を生成するのにハーバー・ボッシュ法が使えるため、この方法の発見によって農作物の収穫量は飛躍的に増加したのです。
化学肥料の誕生以前は、農作物の量が人口増加に追いつかず、人類は常に貧困と飢餓に悩まされていました。
しかしハーバー・ボッシュ法による窒素の化学肥料の誕生や過リン酸石灰によるリンの化学肥料の誕生により、ヨーロッパやアメリカ大陸では、人口爆発にも耐えうる生産量を確保することが可能となったのです。
ハーバーは本法の業績により、1918年にノーベル化学賞を受賞、またボッシュは本法を応用した高圧化学反応の研究により、1931年にノーベル化学賞を受賞しています。
この方法は同時に、平時には肥料を、戦時には火薬を空気から作るとも形容され、爆薬の原料となる硝酸の大量生産を可能にしたことから、その後の戦争が長引く要因をも作りました。
その例ですが、ドイツ帝国は、第一次世界大戦で使用した火薬の原料の窒素化合物の全てを国内でハーバー・ボッシュ法を元にして調達できたのです。
一方、本法によるアンモニア合成法の開発以降、生物体としてのヒトのバイオマスを、従来よりもはるかに多い量で保障するだけの窒素化合物が、世界中の農地生態系に供給され、世界の人口は急速に増加しました。
現在では地球の生態系において最大の窒素固定源となっています。
さらに、農地生態系から直接間接双方の様々な形で、他の生態系に窒素化合物が大量に流出しており、地球全体の生態系への窒素化合物の過剰供給をも引き起こしています。
この現象は、地球規模の環境破壊の一端を成しているのではないかとする懸念も生じていますが、これについてはまだ良く分かっていません。
国際宇宙ステーション「きぼう」を見よう!
今週前半は太平洋側を中心に晴れる日が多い予報です。
空気が乾燥すると、空気が澄んで、星や惑星が一層きらめいて見えます。
星々と共に野口聡一さんも乗る国際宇宙ステーション「きぼう」も見られそうです!
見られる日にちや時間は・・・
国際宇宙ステーション・ISSは、木星より強い輝きで見えることもあり、速度も飛行機より少し遅いくらいで、肉眼で捉えやすいとのことです。
ISS自体が光っているのではなく、太陽の光を受けて光って見えるため、太陽が当たる時間や軌道などと合わせて、観測に最適な日があるようです。
とりあえず、今日と明日ですが・・・
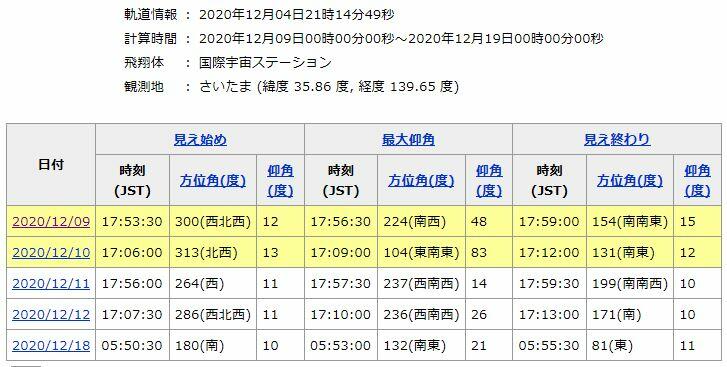
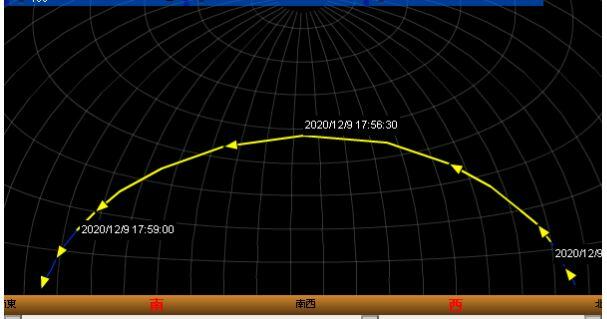
<9日(水)午後5時52分頃の目視予想>
西日本や東日本(四国・中国~北陸や関東)では、9日(水)の午後5時50分過ぎから午後6時前までで、高度が高く、かなり見えやすくなりそうです。
東日本はやや雲が多いものの、西日本はよく晴れるので、観測に最適となりそうです。
関東は、昨日8日の方が観測しやすかったようですね・・・
12/9(水)17:50ごろから
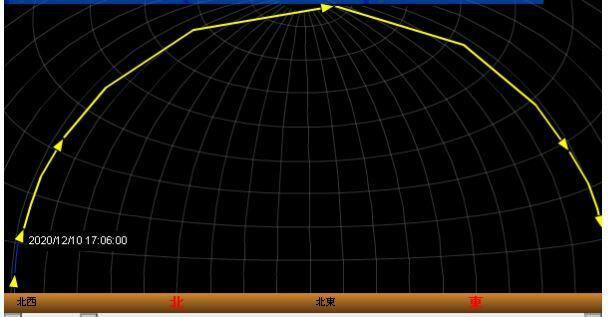
12/10(木)17:05ごろから
この他にも観測しやすい日は、一年を通して地域ごとにあり、それぞれ異なっています。
今日見えなくても、観測のチャンスはまだありますよ!
JAXAのホームページ、きぼうをみよう(http://kibo.tksc.jaxa.jp/)から調べてみてください。
「きぼう」が見えますように!
はやぶさ2 生命の起源有機物見つかるか?
Q.なぜ小惑星を探査するのか?
A.小惑星を探査するのは、それによって「太陽系の起源と進化」と「生命の材料(有機物)の進化」という根本的ななぞの理解が進む と期待されているからです。
「はやぶさ2」では、太陽系形成初期の情報を保持しており、しかも有機物と水の存在しているC型小惑星(リュウグウ)から試料を採って帰ります。
それは、人間がこれまで手にしたなかで最も始原的なものであり、地球の汚染もありません。
したがって、試料を分析し、その結果を試料の地質情報(小惑星の構造・物質分布・熱の様子などの情報)ととも に読み解くことによって、以下のような研究を大きく進めることができると考えられています。
(1)生命の材料(有機物)は地球で進化したのか、小惑星などの宇宙から輸送されてきたのか?
(2)小惑星では有機物はどのように進化したのか?
(3)地球の海水はどこから供給されたのか?
(4)太陽系の材料はどのようなもので、どのように形成され、どのような進化を遂げたのか?
Q.なぜ小惑星には太陽系ができたころの痕跡が残っていると考えられるのか?
A.地球の岩石や砂を調べても太陽系のできたときの姿はわかりません。
地球をつくった元の物質は地球が誕生する過程でどろどろに溶けてから固まっているため、そのころの 情報は失われているからです。
一方、リュウグウのような小惑星は熱的な影響は小さく、昔の状態をよく保持していると考えられます。
Q.なぜリュウグウがターゲットとして選ばれたのか?
A.主に以下の3つの理由からです。
(1)C型小惑星(有機物や水を多く含む、始原的な天体)のひとつであるからです。
(2)微惑星の衝突破壊で生成された破片天体と推定されているので、微惑星を作った物質が 何なのかを直接に確かめることができます。
(3)軌道はほぼ地球と火星の間に収まっているので、地球から比較的短い距離で到達できます。(C型小惑星の多くは火星と木星の間にあります)
太陽系と生命の起源と進化のなぞを明かす試料の分析
太陽系と生命の起源と進化のなぞの解明という壮大な目的のためには、リュウグウより採ってきた試料の分析が決定的に重要です。
まず重要なのは、リュウグウで採取した試料をそのままの状態で物質や熱の汚染なしに地球まで持ち帰ることです。
試料を格納するサンプルキャッチャーは、3カ所から採取された試料が混ざることなく、3部屋で個別に保管される構造を持っています。
サンプルコンテナは、サンプルキャッチャーを完璧に密封して保管し、地球に帰還す る構造を持っています。
地球に突入すると空気との摩擦で表面は最高で3000℃になりますが、内部は最高でも50℃以下に保たれます。
このようにして地球へ持ち帰った試料の初期分析は6つの国際チームによって行われます。
このうち3チームのリーダーが九州大学の先生方です。
東北大学の中村教授も以前は九州大学の所属でした。
「はやぶさ2」の試料分析では九州大学が世界をリードしていると言えます。
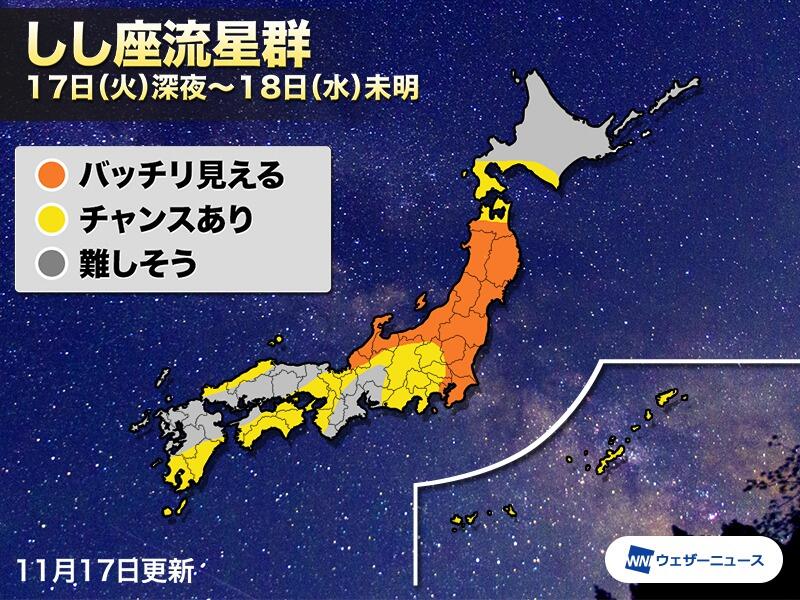
今日深夜から明日未明に獅子座流星群
今日11月17日、しし座流星群の活動が極大となります。
予測極大時刻は17日20時ごろですが、このときには放射点が地平線の下なので、しし座が昇ってくる18日未明から明け方ごろが一番の見ごろとなるそうです。
月明かりの影響はないようですが、活動は低調とみられるので、空の条件の良いところでも1時間あたり5~10個程度とのこと。
観測は防寒の準備を万全にして。
21日の未明に別の出現ピークが見られるという可能性の予報もあるので少し気にかけておきたいですね。
これまでも大出現で有名なしし座流星群ですが、
テンペル・タットル彗星の通り道を毎年この時期に地球が通過し、そこに残されていた塵が地球の大気に飛び込んで上空100km前後で発光して見える現象だそうです。
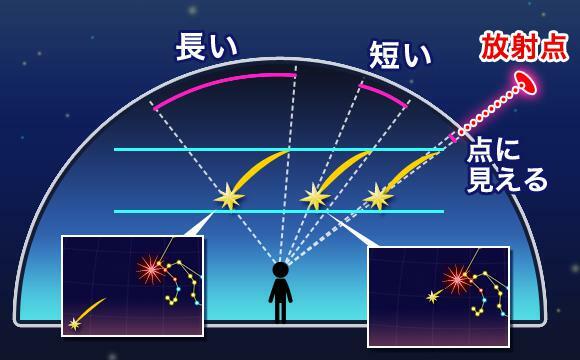
しし座流星群の特徴は?
(1)スピードが速い
しし座流星群の流れ星の速度は秒速71kmに達し、国際天文学連合がまとめた64の主要な流星群の中で、最もスピードが速い流星群とされています。
よく、流れ星が流れている間に3回願い事をすると叶うと言われていますが、願い事を唱えるのが一番難しい流星群とも言えそうです。
(2)明るい流れ星が多い
しし座流星群は全体的に明るい流れ星の割合が高く、火球と呼ばれるひときわ明るい流れ星も多く観測されます。
(3)流星痕が観測できることも
明るい流れ星が流れた後、その流星の軌跡上で雲のようなものが淡く輝く「流星痕」を観測できることがあります。
しし座流星群は明るい流れ星が多いため、流星が流れた「あと(後・跡・痕)」にも注目して観測するのも良さそうです。
地球衝突!? 小惑星への対策は?
「地球衝突!? 小惑星への対策は」
JAXA 宇宙科学研究所 准教授 吉川 真
天体の地球衝突が現実に起こっています。
最近では、4年前の2013年に、ロシアのチェリャビンスク州に落ちた隕石があります。
このときには、100キロメートル以上にわたって、建物の壁や窓ガラスが壊れ、1500人以上の人がけがをしました。
落ちてきた隕石は20メートル程度の大きさと言われており、発生した衝撃波によって被害が広範囲に及びました。
さらに100年ほど前の1908年には、シベリアでツングースカ大爆発と呼ばれる出来事がありました。
このときには、森林が約2000平方キロメートルにわたって被害を受けていますが、その原因は大きさが60メートルくらいの天体の衝突だと言われています。
地球の歴史、あるいは生命の歴史を見ると、今から6600万年くらい前に、恐竜をはじめとして多くの生物種が絶滅しましたが、その原因として最も注目されているものが天体の衝突です。
大きさが10キロメートルくらいの天体が、メキシコのユカタン半島付近に衝突して、その後、地球の環境が変化しました。
その変化した環境に適応できなかった生物が滅んだというわけです。
大きさが数十メートルくらいの天体でも地球に衝突すれば地域的には大きな被害を受けますし、大きな天体ですと人類絶滅につながるかもしれない・・・ということが1990年代から広く認識されるようになり、天体の地球衝突という問題に対応する活動が始まりました。
これがスペースガードあるいはプラネタリー・ディフェンスと呼ばれる活動です。
スペースガードの活動で重要なことは、地球に衝突する可能性がある天体を発見して、その軌道を正確に把握することです。
天体の軌道が正確に分かると、計算によってその天体が地球に衝突するかどうか、そしてもし衝突する場合には、いつどこに衝突するかが完全に予測できます。
これは、何十年も先の日食や月食が正確に予報できるのと同じです。
つまり、天体衝突による災害というものは、その天体さえ発見して軌道を推定しておけば、完全に予測可能な災害なのです。
地球に接近しうる天体のことをNEO(ニア・アース・オブジェクト)と言います。
具体的には小惑星とすい星(ほうき星)がありますが、1990年代から多くのNEOが発見されるようになりました。
小惑星は、現在すでに73万個以上も発見されています。
その中の、NEO地球に接近しうる小惑星は、約1万6000個が発見されています。
これら発見されている小惑星につきましては、軌道が計算されており、少なくても今後100年くらいは地球に衝突する恐れはないことが分かっています。
しかし、まだまだ発見されていないNEOがたくさんあるのです。
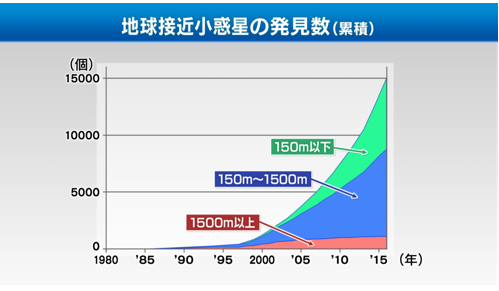
こちらの図には、地球接近小惑星の発見個数の推移が示されています。
このように年を経るごとに発見されている地球接近小惑星の数が増えていくことが分かります。
ただし、大きさが1500メートル以上のものについては、最近はあまり増加していないことも分かります。
これは、この大きさの地球接近小惑星がほぼ発見し尽くされてきたことを意味しています。
ところが、それより小さなものはどんどん数が増えていますから、まだ未発見のものが多いわけです。
まずは、未発見の天体を見つけて軌道を推定することが重要です。
では、もし地球に衝突する天体が発見されたらどうしたらよいでしょうか?
2017年5月に、スペースガードについて議論をする国際会議が東京で開催されました。
この会議では、大きさが300メートルくらいの天体が東京に衝突するという設定で議論が行われました。
もしこのような衝突が起こると東京は壊滅状態になりますから、是が非でも衝突を回避する必要があります。
小惑星のような天体が地球に衝突するのを回避するために、いろいろな方法が提案されています。
その中で、現時点で技術的に可能な方法は、宇宙船のような人工物体を小惑星に衝突させてその軌道をずらす方法です。
映画によくあるように、地球に衝突してくる天体を爆破するのは意味がありません。
仮に天体を爆破できたとしても、破片が地球に降ってくるので被害を回避することはできないからです。
天体を爆破するようなことはせずに、その軌道を変えることが適切な衝突回避策になります。
しかし、宇宙船を衝突させたとしても小惑星の軌道の変化はごくわずかです。
したがって、なるべく早めに対処する必要があります。たとえば、ある小惑星が20年後に地球に衝突するとして、今のうちに宇宙船をその小惑星に衝突させて軌道を少しずらしておきます。
すると、20年後にはそのずれが大きくなって地球に衝突せずにすむというわけです。
すでに米国では彗星に探査機を衝突させるミッションを行っていますし、日本も「はやぶさ」探査機を小惑星に送ることに成功しています。
ですから、技術的には十分可能です。
ただし、この方法は、天体衝突までに十分な時間があることに加えて、相手の天体があまり大きくない場合でしか有効ではありません。
地球に衝突してくる天体の大きさが数百メートルくらいまででしたらよいのですが、それより大きいと、宇宙船を衝突させたくらいでは小惑星の軌道は変化しないのです。
衝突してくる天体が大きい場合には、より大きな力で小惑星の軌道を変える必要があります。
これは、エネルギー的に考えると、核エネルギーに匹敵します。
実際、小惑星の軌道を変えるために核爆弾が使えるかどうかの研究もなされています。
本当に地球衝突がある場合には、いろいろな手段を検討することになるかと思いますが、現時点では核の使用については慎重であるべきだと思います。
天体の地球衝突というと衝突回避が注目されがちですが、天体衝突という情報が流れたときに人々がパニックに陥らないかとか、経済的なダメージはどうなるのか、さらには衝突回避を誰が行うのか、そして仮に衝突回避に失敗したら誰が責任を負うのかなど、複雑で難しい問題がいろいろとあります。
大きな災害を伴う天体の地球衝突は、めったに起こることではありません。
しかし杞憂ではなく、いつの日か必ず起こることです。
いたずらに恐怖心をあおることなく、冷静で着実な対応を進めていくことが重要です。
天体の地球衝突は、天体を発見しその軌道を把握しさえすれば、完全に予測可能な自然災害なのです。
マンホール内での中毒事故
昨夜、茨城県土浦市で下水道の汚泥を取り除く作業にあたっていた作業員の方2人が相次いでマンホールの底に転落し、亡くなりました。
これまでの調べによると、作業員Aさんは下水道内での作業を終えて地上に出ようとした際にマンホールの底に転落し、助けに向かおうとした作業員Bさんも転落したということです。
消防によると、現場からは猛毒の硫化水素ガスなどが検出されたということです。
この2人の方は、作業を終えてさあ帰ろうとしていた矢先だったと思われ、本当に痛ましい事故だと思います。
マンホール内での硫化水素発生の事故は時々耳にしますし、また自分も、下水付近で硫化水素の臭いに気づくことが時々あるんです。
下水で硫化水素が発生するのはなぜなのでしょうか?
原因を調べてみました。
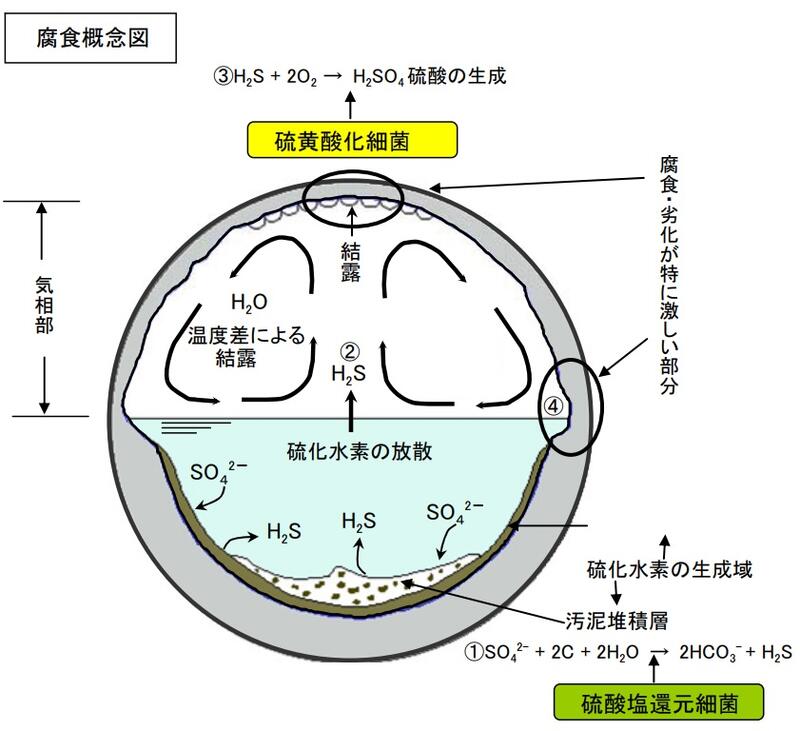
下の図は、下水管が腐食される時の概念図です。
下水中の硫酸イオンSO42-は、ごく普通に存在するようです。
でも、この硫酸イオンが炭素Cと水H2Oに接触し、細菌(硫酸塩還元細菌)の働きで硫化水素H2Sに還元されてしまうというのは、本当に驚きですね!
安定な硫酸イオンに変化していくのが、通常の環境での反応だと思います。
酸素の少ない環境では、嫌気性のこの細菌がこのような反応を起こさせるんですね!
そして、発生した硫化水素は、酸素の多い環境では、今度は好気性の硫黄酸化細菌により一気に硫酸H2SO4に酸化されるということのようです。
ここで生じた硫酸は、下水管やマンホールのコンクリートや鉄筋を腐食する害を生み出すんですね。
換気の悪い下水周辺、または汚泥や汚水が溜まっているような場所では、「猛毒の硫化水素ガスが普通に発生している可能性がある」ということは頭に入れておいた方がいいと思います。
神奈川県の異臭騒ぎのこと
ここ数日神奈川県内で異臭騒ぎが相次いでいます。
今日のニュースで知ったんですが、この異臭は6月から続いているそうです。
「ガスのような臭いがする」「ゴムが焼けた臭いがする」といった通報が寄せられているそうです。
この事件について、周辺の大気を採取し分析を進めていた横浜市が13日に会見を開きました。
「ガソリン等の燃料の蒸発ガスに含まれるイソペンタンやペンタン、ブタンといったものが、通常の大気中に比べて高い濃度で検出された」
「また、化学製品の原材料や物を燃焼した際に発生するエチレンやアセチレンも検出された」
ということです。
異臭の発生源は現時点では不明で、直ちに健康に影響を及ぼすことはないということも発表されました。
さて、検出された物質は、すべて高校教科書でも出てくる比較的炭素数の少ない炭化水素です。
①ペンタン C5H12(CH3CH2CH2CH2CH3)
②イソペンタンC5H12(CH3CH2CH2(CH3)2)
③ブタンC4H10(CH3CH2CH2CH3)
④エチレンC2H4(CH2=CH2)
⑤アセチレンC2H2(CHΞCH)
①、②は揮発性の高いベンジンのような液体で、気化した気体はベンジンやガソリンのような臭いがします。
また、④は気体で、かすかに甘い臭いがしますが、熟れた果物もこの気体を発しているので臭いを想像できるのではないでしょうか?
残りの③、⑤は無臭の気体です。
アセチレンには臭いがあると経験している人がいるかもしれませんが、カルシウムカーバイドと水の反応で生じたアセチレンガスは臭いのある不純物を含んでいるのです。
純粋なアセチレンは無臭です。
ということで、「ゴムが焼けた臭い」に関連するような物質はなさそうですよね?
異臭の原因がはっきりと究明されて欲しいと思っています。
火星大接近
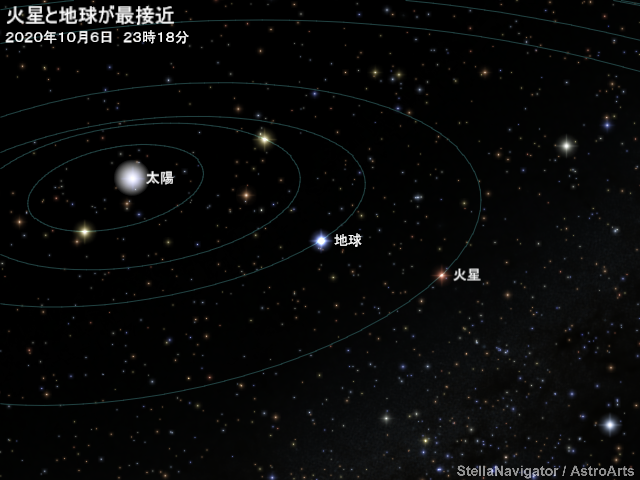
明日10月6日夜、火星が地球に大接近します!
夜11時18分に最接近とのことです。
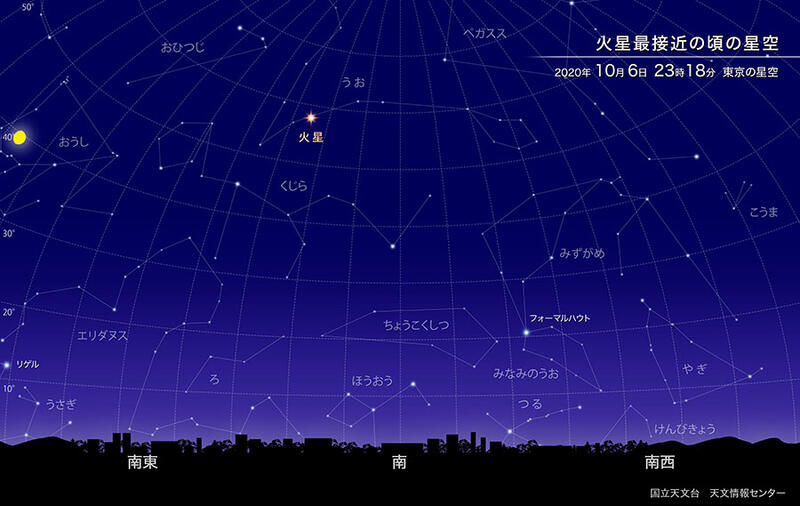
夜空を見上げた時、火星の位置関係は以下のようになるそうです。
色や明るさなど、どんな感じに見えるのでしょうか?
台風10号が予想よりも勢力を弱めた理由
未曽有の強さと予測されていた台風10号が去っていきました。
亡くなられた方、怪我をされた方、行方不明の方は100名以上いらっしゃるようです。
ただ、不幸中救われたことがあったと分析されていました。
それは、台風が予想のようには成長しなかったことだというのです。
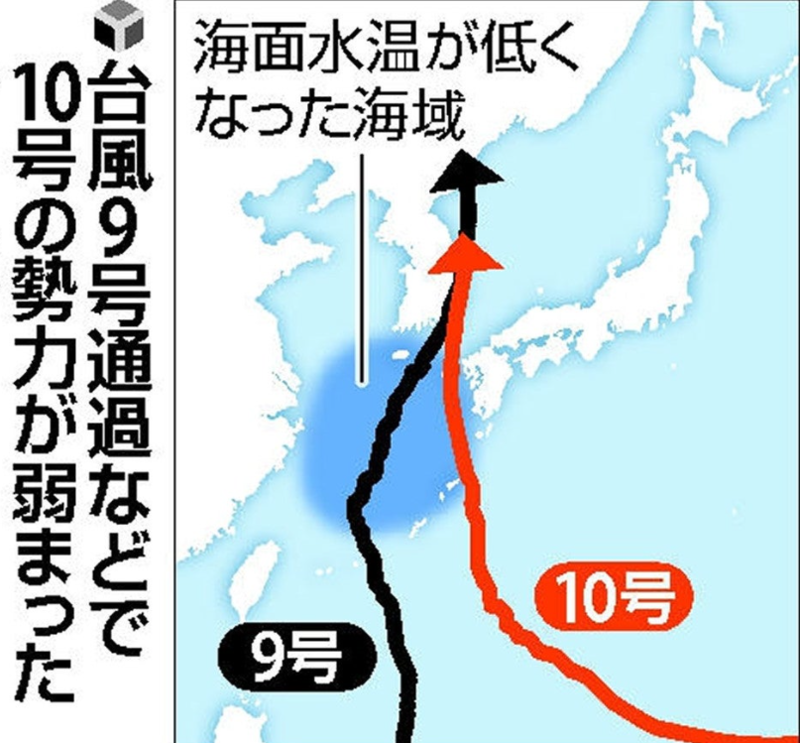
台風10号が当初の予想よりも勢力を弱めた理由について、専門家は、直近に同じようなコースをたどった台風9号の影響で海面水温が下がり、「動力源」となる水蒸気を十分に取り込めなかったためとみている。
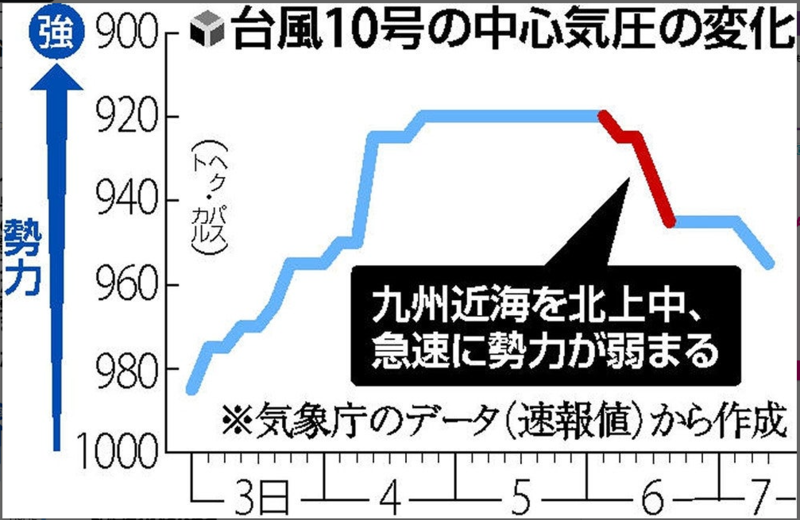
10号は6日午前に奄美地方へ接近しながら急速に衰退。中心気圧が945hPaに上がり、特別警報の発表は見送られた。
勢力が弱まった主な要因として、海面水温の低下が挙げられる。
気象庁によると、8月の九州近海の海面水温は熱帯並みに高かったが、9号が通過した9月2日頃を境に低下したとみている。
海上を台風が進むと、海面近くの温かい水と深い場所の冷たい水が強風でかき混ぜられたり、雨雲に日光が遮られたりして水温が下がる。
勢力が少し弱まったタイミングで水温の低い海域を通ったことで、衰退が加速したのではないかと考えられる。
水温低下に加え、上空の気流が影響し、台風の構造が崩れやすくなったことも一因になった可能性がある。
住宅用れんがに電気を貯蓄 研究第1段階成功!
住宅用の質素なれんがを、電気を貯蓄できるコンデンサーに生まれ変わらせる研究の第1段階が進み、将来、建物が文字通りの発電所になるのではないかとの期待が高まっている。
この新しい技術で活用されているのは、焼成された赤れんがが持つ多孔性の性質だ。
れんがの小さな穴を、電荷を蓄えられる導電性プラスチックでできた微小ナノファイバーで満たしたところ、れんがに小さなライトが点灯する程度の電力を蓄えることができた。
容量を上げることができれば、現在使用されているリチウムイオン電池に取って代わる可能性がある!
「電力れんが」は電気二重層キャパシタ (コンデンサ)だ。
電気二重層キャパシタは、静電荷として電気を固形物に貯蓄する。
利点は、充電・放電がバッテリーよりも速い点だが、今のところ、蓄電量はほんのわずかだ。
電気二重層キャパシタのエネルギー密度とバッテリーの充電速度を上げる研究が世界中で進められている。
より効果的に蓄電する方法の発見は、気候危機対策で極めて重要となる。
再生可能エネルギーは潤沢であっても発電が断続的であるので、そうした電気エネルギーを必要な時まで保存しておけるようにする技術開発は非常に有意義である。
住宅の屋根にある太陽電池は、電力をどこかに貯蓄しなければならず、現在そのためにバッテリーが使われている。
今回の第1段階の電力れんがのエネルギー密度は、リチウムイオン電池のわずか1%しかない。
金属酸化物などの素材を加えることで、れんがの電気貯蓄量は10倍に増やすことができると考えられている。
これが実現すれば、電力れんがが商業化される可能性もある。
最終目標は、エネルギー密度をリチウムイオン電池と同じレベルにすることだ。
「これができれば、この技術はリチウムイオン電池よりずっと安価になる」とダーシー准教授。
「実現できたら、別世界になる。リチウムイオン電池は廃れてしまうだろう」
リチャード・マクマホン教授は、非常に興味をそそられる研究だと述べた。
「エネルギー貯蓄の中でも、とりわけ電力の貯蓄は、現代において大いに関心を持たれている。
しかし今回の研究は、可能性を興味深い形で示したものではあるが、実用化はまだかなり先になる」
コロナ重症化防ぐ可能性?
大阪府の吉村知事と松井一郎大阪市長が4日、
市販のうがい薬によるうがいで重症化を防ぎ人に感染させにくくする可能性があると発表した。
会見で吉村氏は、殺菌効果のある成分「ポビドンヨード」を含むうがい薬を使うと「陽性者が減るのではないかという研究結果が出た」と述べた。
【ポビドンヨードとは】
ポビドンヨードは殺菌力、即効性に優れていることから、うがい薬、手指の殺菌、傷の消毒などに世界中で使われている代表的な消毒剤。
コンブやワカメなどに含まれるミネラルの一種であるヨード(ヨウ素)の酸化作用を利用した抗微生物成分。
ヨウ素のアルコール溶液であるヨードチンキなどは人体への刺激が強すぎるため、水に溶けやすくする成分であるポリビニルピロリドン(ポビドン)と合成することで広く普及した。
茶色い液体が特徴。
繰り返し使用すると細菌やウイルスが、その薬に対する耐性を持ち、効き目が落ちる場合があるが、ポビドンヨードは耐性を持った細菌やウイルスにも有効とされる。
妊婦、甲状腺機能に異常がある場合は使用に注意が必要。
鉛蓄電池(カーバッテリー)の過充電で硫化水素が発生する?!
新潟県上越市の上信越道で、25日夕方から26日朝まで舗装工事のパトロールをしていた2人が26日、
駐車していた車の中で意識不明で見つかり、死亡が確認されました。
パソコンや回転灯に使うため車内に積まれたバッテリーから異臭がしていたということです。
異臭の原因は硫化水素だったようです。
なぜ、バッテリーから硫化水素が発生するのでしょうか。
高校化学での勉強では、鉛蓄電池の充放電の反応で硫化水素H2Sが発生することは教わりません!
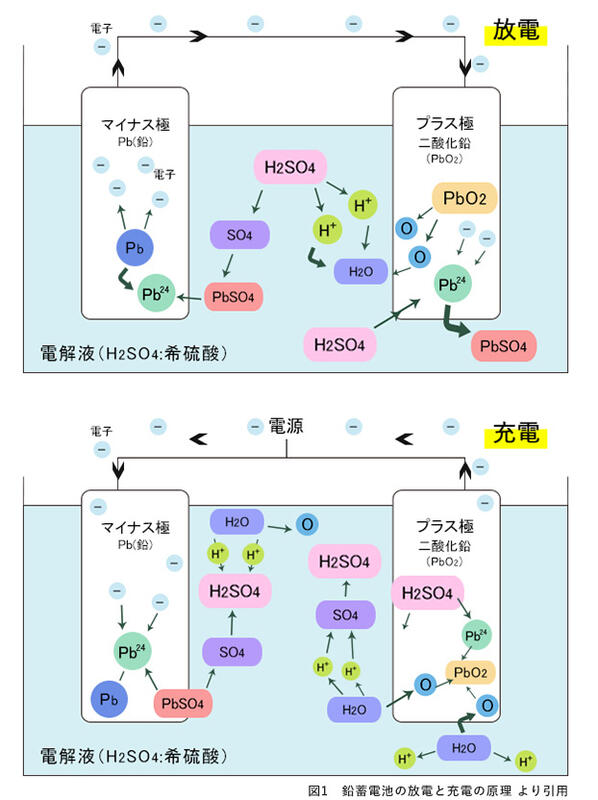
高校化学で学ぶ鉛蓄電池を充電する時に起こる反応は次の通りです。
PbSO4(正極) + PbSO4(負極) + 2H2O → PbO2(正極) + Pb(負極) + 2H2SO4 ・・・①
この反応だけなら硫化水素H2S等の気体は一切発生しません。
この他、通常でも上の図以外に過充電による反応が多少起こっています。
この時水H2Oの電気分解が起こり、気体の水素H2、酸素O2が発生しています。
2H2O → 2H2↑ + O2↑ ・・・②
この時発生する水素に毒性はないものの、空気と共に充満すれば爆発の危険性があります!
過去の経験ですが、父親がスクーターのバッテリーの充電をしている際、自分がショートさせてしまい、バッテリー上部が破裂して壊れてしまったんです。
バッテリー内部の電解液上部の空間に溜まった水素と酸素の混合気(爆鳴気ですね!)に電気火花で引火させてしまった訳ですね。
また、発生する細かい気泡が液面ではじける時、希硫酸の霧も生じることになります。
でも、ここでも硫化水素ガスは発生していません。
調べてみましたが、詳しい反応は見つけられませんでした。
考えられるのは、充電は電気分解であり、電気分解は強制的に酸化還元反応を起こさせる操作です。
上記①の反応だけなら、酸化還元を受けている元素はPbだけですが、
②の反応が起こる時は、酸化還元を受ける元素はH、Oにも及んでいます。
こんな具合で、さらに条件が変化すれば、希硫酸H2SO4中のSが還元されることも考えられます。
H2SO4 → H2S が起こった時、Sの酸化数は+6 → -2 と非常に大きく変化しますが、電気分解なら充分考えられることだと自分は思います。
さて、では、この鉛蓄電池(カーバッテリー)の使用について、通常どのような注意が必要なのでしょうか?
<通常の車載使用では>
充電中は水素ガス、酸素ガス、酸霧(希硫酸)が少量ですが発生しています。
これらの物質によって付近の物が影響を受ける恐れのある場合は特に配慮が必要ですが、
当初から車載されている状態なら、自動車メーカー側で対策がされているので、ほぼ心配は無いと考えられます。
バッテリーからの発生物質は外部へ放出され、また過充電されにくいよう電気的に制御されています。
<特殊な使用状況では要注意!!>
バッテリーが古い、バッテリー液が少ない、過充電する、等の条件によっては、まれに硫化水素が発生します。
今回の死亡事故では、「ソーラーパネルによる過充電」「バッテリーを密閉された室内に設置」といった条件が重なって起こったようです。
特に、特殊な使い方をする場合は、今回の事件を踏まえて充分に注意すべきでしょう。
「スーパームーン」! 8日夜に見えるかも!
8日は、地球と月の距離が近付き、満月が大きく見える「スーパームーン」となる。
気象庁によると、同日は西日本の一部を除き、やや雲の多い空模様となる見通しだが、
夜空に晴れ間が広がれば普段より明るく輝く満月が見られそうだ。
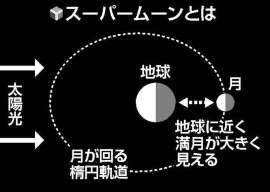
月は、地球の周りを楕円軌道で回っている。
8日には約35万7000キロメートルまで近付くため、今年最も地球に近い満月となる。
国立天文台によると、今年最も遠い満月(10月31日)に比べ、見かけの直径は約1.14倍となり、約30%明るく見えるという。
「新型コロナウイルスの影響で外出しにくい状況なので、大きい満月を見て元気を出してもらえれば」とのことです!
PS.7日の今夜も見えていますよ!
物理基礎の考査得点訂正等、すべて確実に終了しました
学校での訂正点の入力、成績処理の修正等、すべて完了しました!
今回の件は、事前のチェックが不充分でミスを生じてしまい、
申し訳ありませんでした。
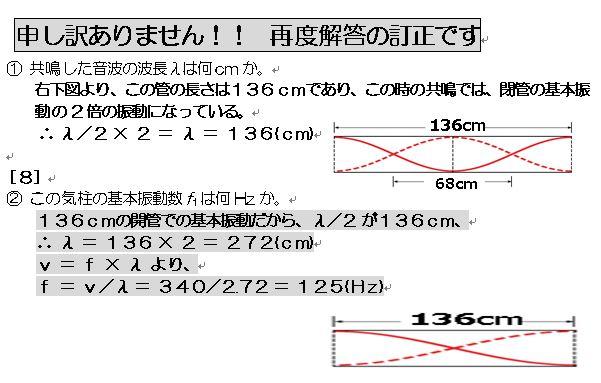
再度、解答の訂正(申し訳ありません!!)
恥ずかしく、本当に申し訳ないのですが、
訂正した解答が間違っていました・・・!
訂正箇所は、[8]の②です。
当初の訂正解答では、①の状態の振動数を出してしまっていました。
しかし、問題は、「この気柱の基本振動数は・・・」と聞いているのですから、
この136cmの気柱での基本振動数を計算しなければいけませんね!
これについての対応ですが、
この②の解答が125Hzで✖が付けられているものだけでいいですから、写メを添付して岡本にメールして下さい。
明日16日(月)10時までに送って下さい!
なお、①の状態の振動数250Hzも正答として扱いたいと思います。
本当に申し訳ありません!!
物理基礎得点の訂正処理について
今朝、この件について当サイトに掲載しましたが、すでに皆さんから多数のメールが届いています。
もうしばらくメールを待って、明日15日午前中にまずはこちらの自宅で訂正処理をして、各自へメールを送りたいと思っています。
そして、16日(月)午前に学校での訂正点の入力を完了させたら、このサイト上に訂正完了を報告します。
今回の件が、まだ全員に伝わってないかもしれません。
もし伝達がまだされていなければ、皆さんから、クラス内のメンバー全員に情報伝達をお願いします!
該当クラスは、1、4、5、6、9組です。
自分のクラス以外の横のつながり(部活等)での連絡もしてくれると、全員に確実に伝わると思います!
物理基礎考査の解答の間違いについて(現2年生は必ず見て下さい!)
昨日、テストが返却されたと思いますが、
こちらの解答が一部間違っていました!
お詫びして訂正します。
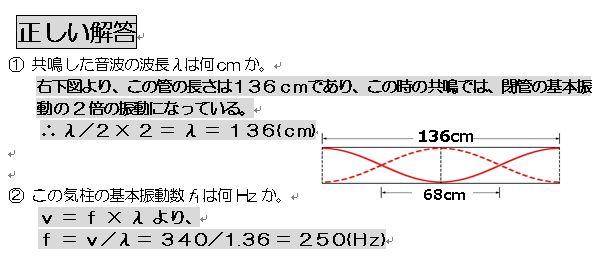
正しい解答は以下のようになります。
申し訳ありません!!
至急、対処したいと思いますので、「各自の答案のこの部分を氏名欄が含まれるように写メして」、岡本のアドレスに添付送信して下さい!
※ 対象者は正解になる生徒だけでOKです。
※ これを見た人は、クラスや仲間の LINE 等で連絡を回してくれると助かります!
※ 点数の訂正が出来るのは、3月16日(月)の10時までです! 遅れないようにメールして下さい!
(管の長さが68cmという問題を作るつもりが、節と節の間が68cmとしたままだったので、こういうミスをしてしまいました!でも、見直しをしっかりしていれば、こんなミスは起こりませんね! ゴメンなさい!!)
休校中の子供たちにぜひ見て欲しい科学技術の面白コンテンツ
科学技術広報研究会から公表された、臨時休校対応特別企画です!
https://sites.google.com/view/jacst-for-kids/home
面白いですよ!
ぜひ覗いてみて下さい!
まずは、さっと見られる映像からどうぞ。
メニューは下のような感じです。
(これはスクリーンショットです。リンクは上からたどって下さい)

吉野彰博士の開発した電池の、大きな可能性
リチウムイオン電池の生みの親、旭化成名誉フェロー吉野彰博士が2019年の日本人ノーベル化学賞に輝きました!!
あえて研究を始められた頃の写真を使わせていただきました!
高性能電池が開発されることの意義、そして高性能電池の大きな可能性について調べている最中なんです。
蓄電池は、電気を溜めることが出来る電池ですが、身の回りに充電が出来る電池は沢山ありますよね?
しかし、非常に大量の電気を溜めることが出来る電池を自由に使えるようになると、今までの電池とは違った画期的な利用法が考えられるのではないでしょうか?
では、具体的にどのようなメリットが生じてくるのか?
ここのところが、明るい未来への展望を実感できる要因ではないかと思っているんです!
このウェブサイトは、
NetCommons3.3.7で動いています。
NetCommons プロジェクト 開発の、
CMS+グループウェアです!
| 日 | 月 | 火 | 水 | 木 | 金 | 土 |
27 1 | 28 1 | 29 | 30 | 31 | 1 | 2 |
3 | 4 | 5 | 6 | 7 | 8 | 9 |
10 | 11 | 12 | 13 | 14 | 15 | 16 |
17 | 18 | 19 | 20 | 21 | 22 | 23 |
24 | 25 | 26 | 27 | 28 | 29 | 30 |