理科のこと、環境ニュース
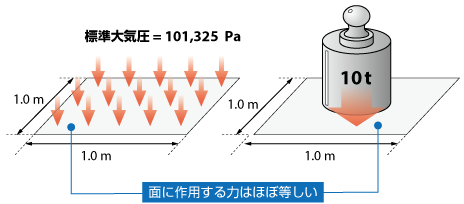
100平方センチメートルの面積にかかる大気圧による力は?
以前、「1辺10センチの正方形にかかる大気圧による力の大きさはどれくらいか?」
と問題にしましたが、その解説を書きたいと思います。(遅くなってすみません)
まず大気圧の大きさですが、1013hPa(ヘクトパスカル)と覚えていると思います。
ここでのh(ヘクト)は単位の接頭辞で、100を表しています。
すると、
1013hPa = 101300Pa
これは約100000Pa(10万パスカル)
となりますね。
また、1Pa(パスカル)の定義ですが、1m2の面積に1N(ニュートン)の力が加わる大きさの圧力となっています。
さて、1kgの質量の物体にかかる重力の大きさ(つまり重さ)を考えてみます。
W = mg = 1kg × 9.8m/s2= 9.8kg・m/s2=9.8N ≒ 10N
となるので、
1kg重 ≒ 10N
ということは、
1N ≒ 0.1kg重
となります。
ですから、こう覚えておくといいと思います!
「1Paとは、1平方メートルに約100グラム分の重さがかかる圧力」
そして、大気圧1013hPaは、
「1平方メートルに約1万キログラム分の重さがかかる圧力」
となりますね!
次は、1辺10cmの正方形の面積をm2単位で求めてみましょう。
10cm=0.1m
ですから
(10cm)2=(0.1m)2
よって
100cm2=0.01m2
となります。
さあ、最後の答えを出してみましょう!
1辺10センチの正方形にかかる大気圧による力の大きさは?
100000Pa × 0.01m2 =1000N
そして、この1000Nは、約100kg重となります!
「1辺10センチの正方形にかかる大気圧による力の大きさは約100kg重!」
ちょっと信じられない重さだと感じませんか?
そして1平方メートルには、この100倍の10000kg重つまり10トン重の重さが加わっていることになるんですね!
結露で校舎内の床が広範囲に濡れる
今朝の校舎内の床、特に廊下の床面は結露のため広範囲に濡れていました。
校舎内の、特にコンクリートにリノリウムを貼った「冷たい床」は全て濡れているような状況でした。
この現象はそれほど頻繁に発生する訳ではないんですが、ちょうど今頃発生しやすいと思います。
外気温が上がってきているんだけど、校舎全体はまだ温まっていなくて壁や床は冷たいくらいの時期ですね。
そんな時期に、雨が降るような蒸し暑い大気が校舎内に入ってくると、大気中の水蒸気が校舎内の冷たい所で結露します。
今日気付いたと思いますが、床だけでなく壁や金属製の手すり、窓枠なんかも濡れていたと思います。
湿度の高い大気が入ってきても、校舎の温度が低くなければ結露は起こらないんですね。
校舎のようなコンクリート製の建物は比熱が大きく、すぐに温まったりすぐに冷えたりしにくいんです。
ということで、急に外気温が上がってその大気の湿度が高い時にこの現象は発生する訳です。
でも、校舎の窓や入口が開いていない時は、気密性が割と高い校舎の中に大気は入っていきません。
登校時校舎の入り口が大きく解放されて、暑いからとたくさんの窓も開けられると一気にこの結露が起こる訳ですね。
梅雨時期でなくても、台風が生ぬるい湿った空気を持ってくる時にも同じようなことが起こります。
台風の時は風が強いので、ドアや窓を閉め切っていても隙間から大気が入り込んできて結露が起きるんです。
今度同じようなことに遭遇したら、良く観察してみて下さい。
床が濡れているのは、外の雨が入り込んできたからではないんですね。
さて今日このような状況で、校舎内で滑りそうになりませんでしたか?
上履きはスリップに対して強くはないと思うので、充分に気を付けて下さい!
スリップして転倒すると大ケガになることもありますから!
シンプルだけど良く考えられた実験(詳細)
前回ざっと書いたこの実験について、原理も含めて記録しておきたいと思います。
フラスコ内の水をしばらくの間沸騰させると、水蒸気が発生しフラスコ内の空気は追い出され水蒸気だけになります。
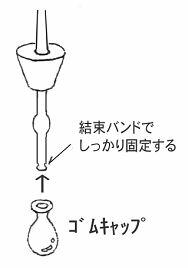
火を止め、フラスコにピペット(俗称スポイト)を刺したゴム栓をはめ込むのですが、このゴム栓はこんな感じに作ってあります。
これをフラスコにこんな感じにセットします。
フラスコ内の温度が下がっていくと、内部の水蒸気は凝縮して液体の水になっていくので、フラスコ内部の気圧が下がっていくことになります。(フラスコ内の気体分子が減っていくから)
するとフラスコ内は100℃を下回っているにもかかわらず水が沸騰することになるんですが、これを減圧沸騰と呼んでいます。
フラスコ内の湯から泡が出ていて沸騰している様子が分かるでしょう?
フラスコの内部がいつも水面を押さえつけていた大気圧より低い圧力となるため、100℃を下回る温度でも沸騰できるようになるという訳です。
「高い山の山頂では気圧が低く、100℃にならずにお湯が沸騰する」と聞いたことがあると思いますが、これと同じ理由です。
ちなみに圧力なべはこの逆で、なべに閉じ込めた水蒸気でなべの内部が高圧になるようにしてあるんです。
こうすると100℃を超えないと水が沸騰出来ないことになり、100℃を超える温度で調理が出来ることになる訳ですね。
さて、減圧沸騰がしばらく続くと水蒸気が新たに生じるためフラスコ内部の圧力は上昇していきますよね。
すると沸騰が収まっていく訳ですが、フラスコと中の湯は外気にさらされ続けているので冷えていく一方です。
下の2つの写真では、水蒸気の凝縮がより多く起こってきてフラスコ内に水滴が沢山付着してきている状況が分かると思います。
さあ、生じた水蒸気が冷えてまたまた減圧沸騰が起こるより早くフラスコ全体が冷えるとどうなるでしょうか?
フラスコ内部の水蒸気が急激に凝縮すると、内部の圧力も急激に減少します。
ここでピペットのゴム球に着目して下さい!
ゴム球の内部は外の大気に通じているのでゴム球内部は大気圧によって外側に押され続けています。
ここでフラスコ内部つまりゴム球外部の圧力がすごく小さくなったらどうなるでしょう?
ゴム球は内側から押されている力で大きく膨らむことになりますよね?!
ごらんの通り、すごく見栄えのするはっきりとした結果になりました!
この実験はやってみた後で気付いたんですが、とても良く考えられているんですね!
まず、ピペットのゴム球の代わりに普通のゴム風船で実験する例があるんですが、風船は軟弱なのですぐ膨らんでしまって減圧沸騰がしっかりと見られないのではないかと思います。
そして、ピペットのゴム球に隙間なく接続できるのはガラスピペットの本体ですよね?
さらに、ピペット本体とゴム球の接続を確実にするために結束バンドを使っていることも良く考えたと思います!
さて、この実験の全体像と原理は見えたでしょうか?
最後に問いを1つ書いておきたいと思います。
1辺10センチの正方形つまり100cm2の面積にかかる大気圧による力はどれくらいだと思いますか?
答えは次回に!
シンプルだけど良く考えられた実験
まずフラスコ内の水を沸騰させます。
火を止め、ピペットを付けたゴム栓をはめます。
放置して冷やすと、少し間をおいて減圧沸騰が始まります。
そして、さらにフラスコを冷やすと、最終的には・・・
さて、こうなる理由は・・・?
CO2排出削減の救世主的技術、二酸化炭素そのものを回収する方法!
すでに大気中に排出されてしまった二酸化炭素CO2、あるいは、これからもまだ排出されるであろうCO2そのものを、どのように除去したらいいのでしょうか?
その最先端技術の紹介です。
自然界における二酸化炭素循環
人類が化石燃料を使う前、地球上においてCO2は基本的に水や酸素と同様に、増えもせず減りもせず、うまく循環していたはずです。
地球化学的循環は数百万年オーダーの変動で、大気中のCO2は水に溶け、やがて炭酸カルシウム(CaCO3)となって固体になり、火山の爆発によりCO2が大気中に出て、また水に吸収されるという循環サイクルが完成します。
生物学的循環は数万年オーダーの変動で、植物は大気中のCO2と水から光合成によりデンプンやセルロースを生成。
この時に酸素が発生し、動物は酸素を吸ってCO2を吐いています。このように、CO2や酸素はバランスよく循環しています。
これが自然の摂理です。
さて、人為的CO2排出ですが、人類最初の化学反応は火を使った燃焼でした。
人類は、火を使って木や草を燃焼させエネルギーを獲得してきました。
木や草は炭素を骨格とした有機化合物からできていますので、燃やせばCO2が発生します。
この燃焼という化学反応は現在でも行われており、重要なエネルギー獲得手段になっているのは周知の通りです。
そして人類は、有機化合物からできている石炭・石油・天然ガスといった化石燃料を大量に燃やし、地球化学的循環や生物学的循環に比べて微々たる短期間、過去200年の間に、一方的に大量のCO2を排出してきました。
この人為的に排出されたCO2はリサイクルされておらず、CO2は大気中に溜まる一方です。
では、CO2はどのように削減すればいいのでしょうか。
二酸化炭素そのものを直接回収するには
今注目を集めているのは、化石燃料をできるだけ使わない、あるいは再生エネルギーの活用などの間接的削減といったことではなく、CO2そのものを直接回収して削減する技術です!
この技術は、ダイレクトエアキャプチャー(DAC)と呼ばれますが、経済や社会活動に制約を与えることなく、CO2だけを削減することができる温室効果ガス削減の救世主的方法と言えるでしょう。
以下、いくつかの研究・開発例を紹介します。
<神戸学院大学・稲垣教授考案>
アンモニア(NH3)など窒素原子を含む化合物であるアミン類がCO2を吸収することは周知の事実ですが、一緒に水を吸収してしまう欠点がありました。
しかし最近、メタキシリレンジアミンを用いると、この欠点を克服できることが見出されました。
吸収されたCO2を取り出すためには一般的には高温が必要ですが、この場合にはCO2吸収後、比較的低温の120℃でCO2を放出しますので、早期の実用化が望まれます。
<公益財団法人 地球環境産業技術研究機構考案>
CO2を吸収する化学吸収液(2ーイソプロピルアミノエタノール水溶液にピペラジン誘導体やエタノールアミン誘導体を含むもの)や、固体吸収材(多孔質のシリカゲルにアミンを担持させたもの)を開発しています。
こうしたCO2を化学的に吸収する方法の開発は重要です。
<日本CCS調査株式会社考案>
現在、日本CCS(Carbon dioxide Capture and Storage)調査が、苫小牧沖の海底1000m以上の深さにある隙間の多い砂岩などからできている貯留層に、製油所から排出されるCO2を大気放出前に回収(活性アミンプロセス)して貯留する実証プラントを稼働させています。
かなり大掛かりな施設ですが、こちらも実用化が期待されます。
<JFEエンジニアリング株式会社考案>
清掃工場から排出される排ガスからCO2を回収して利用するCCU(Carbon Capture and Utilization、二酸化炭素回収利用)プロセスの実証実験を開始すると発表しました。
このプラントのCO2吸収方法も、天然ガスプラント建設等で実績のあるアミン吸収法です。
CO2回収を清掃工場に適用すると、ごみに含まれるバイオマス分を合わせた「ネガティブカーボン(CO2回収量>排出量)」を達成することが可能になります。
<日揮株式会社考案>
セラミック製のゼオライト膜を活用したCO2分離・回収技術の実証試験を米国テキサス州で開始しています。
日本ガイシと共同開発したゼオライト膜は1ナノメートル以下の微細な穴を多く持つのが特長で、ちょうどCO2を通す大きさなので、原油生産時に出てくるメタンなど他のガスから分離することができます。
このウェブサイトは、
NetCommons3.3.7で動いています。
NetCommons プロジェクト 開発の、
CMS+グループウェアです!
| 日 | 月 | 火 | 水 | 木 | 金 | 土 |
27 1 | 28 1 | 29 | 30 | 31 | 1 | 2 |
3 | 4 | 5 | 6 | 7 | 8 | 9 |
10 | 11 | 12 | 13 | 14 | 15 | 16 |
17 | 18 | 19 | 20 | 21 | 22 | 23 |
24 | 25 | 26 | 27 | 28 | 29 | 30 |